溶解係数は、 特定の温度および圧力で 溶媒 を飽和させるのに必要な溶質の量です。
溶液 に関しては、溶質の量が多いほど、溶液の濃度が高くなることに留意する必要があります。さらに、それぞれの物質は一定量の溶媒に飽和しています。
溶解度係数に比べて溶質の量が多い場合は飽和溶液も沈殿する可能性があり、溶解度係数に比べて溶質の量が多い場合は過飽和溶液も沈殿する可能性がありますが、加熱などの外部要因によって沈殿する可能性があります。余分なものを溶かします。特定の 物質は 、温度が異なると溶解度が異なる場合があります。
溶解係数は、溶質分子と相互作用するのに十分な溶媒分子が存在しないため、分子が結合を形成できなくなったときに溶質が過剰になることを分析する場合に役立ちます。同じ溶質でも溶媒が異なると溶解度も異なります。
溶解係数の計算式は次のとおりです: m1/Cs = m2/100
例: 50 °C では、100 g の水に最大 80 g の Ba(NO3)2 を溶解できます。したがって、これはこの温度におけるこの塩の溶解係数です。
Cs=80g/H2O 100g。
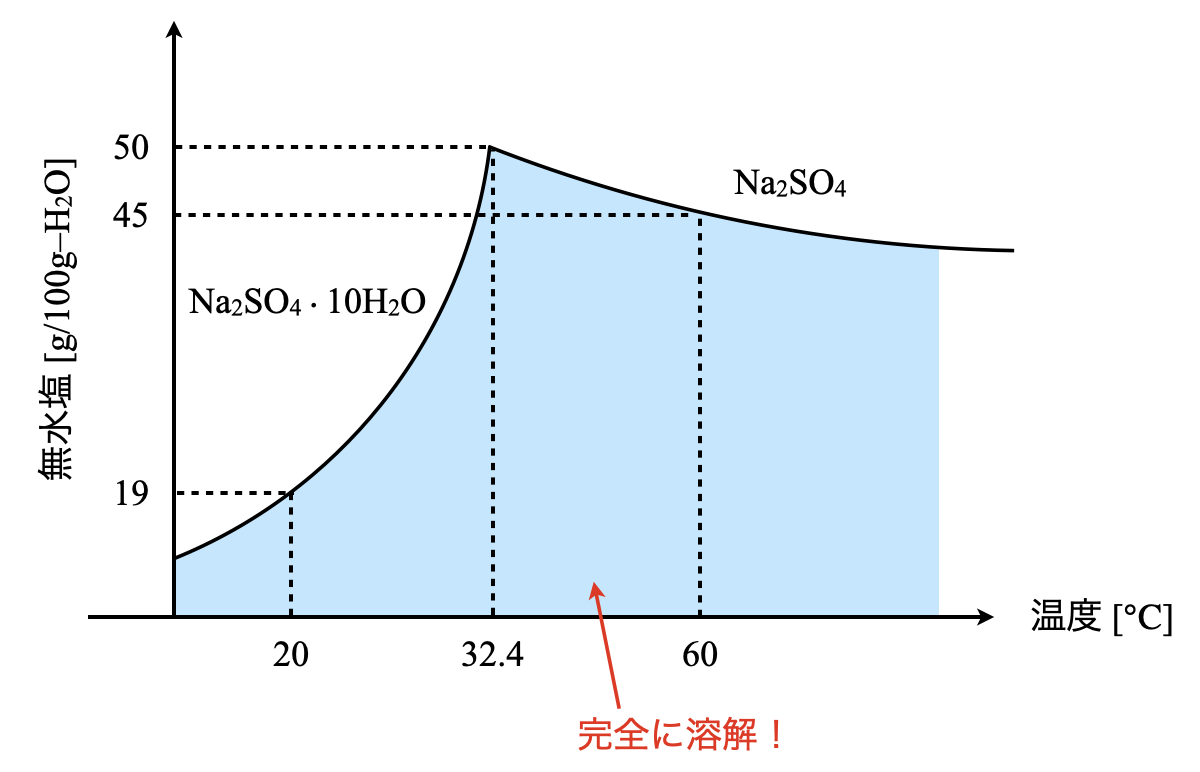
ほとんどの物質は温度が上昇すると溶解度が増加します。ただし、ガスは溶解度が低下します。
上の図では、20℃で最も溶けやすい物質はAgNO3です。 40℃での NaNO3 の溶解度は 100g/100g H2O です。

さらに、以下の練習問題の解決策は、溶解係数の計算を示しています。
塩の溶解度は温度とともに直線的に変化します。 30℃では、この塩 30g は水との飽和溶液 180g を形成します。このような溶液を70℃に加熱すると、飽和を維持するためにさらに45gの塩を添加する必要があります。塩の Cs を計算します。
- a) 30℃
- b) 70℃
- c) 50℃で
水の量は100gを目安としてください。
解決:
a) 30℃
30gの塩と180gの溶液があれば、150gの水ができます。
水 150g —- 塩 30g
水 100g —-x

150x = 3000
x = 塩 20g
30℃での食塩の Cs = 20g/100mL
b)
70℃
30g + 45g = 塩75g、水150g
水 150g —– 塩 75g
水 100g—–x

150x = 7500
x = 塩 50g
70℃の塩のCs = 50g/100mL
w)
30℃ —- 20g
50℃—–×
30x = 1000
x = 33.3g/100mL
答え:
a) 30℃での Cs = 20g/100mL
b) 70℃での Cs = 50g/100mL
c) 50℃での Cs = 33.3g/100mL
したがって、3 つの異なる温度での塩の溶解係数を計算しました。最終結果も変わることに注意してください。
こちらもお読みください:
溶解係数。 <http://www.4shared.com/get/108951227/8f460a6/coefficient_de_solubilidade.html> で入手できます。 3月3日にアクセスしました。 2010年。
問題の解決。 <http://br.answers.yahoo.com/question/index?qid=20090426102354AASm3T9> で入手できます。 3月3日にアクセスしました。 2010年。
ギャラリー