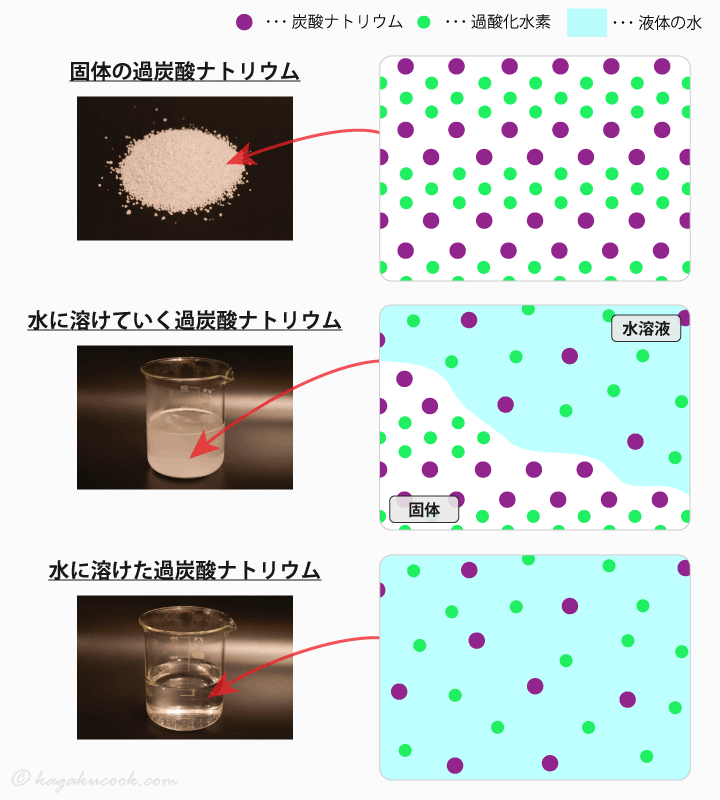
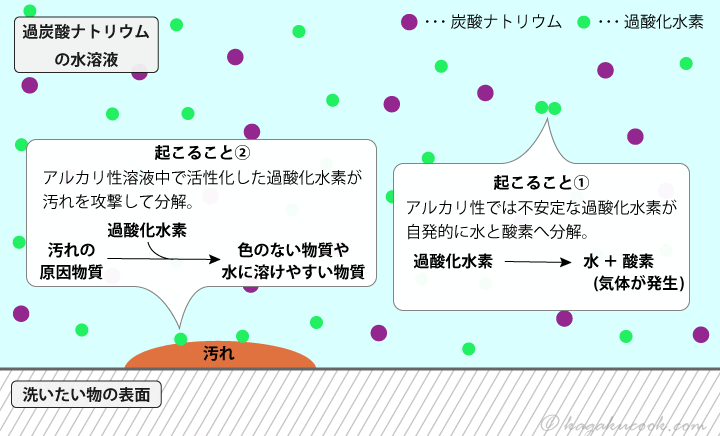
過酸化水素は 過酸化水素 の水溶液です。商業的には、通常、濃度が 3% の溶液中に存在します。純粋な場合、それは粘稠な液体で、密度は 1.46 g/mL、無色で、 硝酸 に似た臭いがあります。融点は2℃、沸点は85℃です。一般の水にあらゆる割合で溶けます。

不安定な化合物であり、主に塩基性媒体中では常温で分解します。溶液は常に酸性媒体(通常は リン酸 で酸性化)で販売されます。金属、石炭、または微粉末二酸化マンガンの存在下では、非常に 発熱する 過程で容易に分解し、発泡します。 過酸化物 に対する酸の作用によって得られます。
実験室では酸化剤として、工業では漂白剤として、医学では消毒剤として、芸術では黒ずんだ絵画や黄ばんだ紙の修復に使用されます。

このような溶液は、体積で表したさまざまな濃度で市販されています。つまり、溶液は分解すると非常に多くの体積の 酸素 を供給します。市販の 過酸化水素 水溶液の濃度は、溶液 1.0 cm 3 を分解して得られる O 2 の体積数で示されます。したがって、10 体積の過酸化水素は、完全に分解すると、体積で使用した水の 10 倍の量の O 2 を放出します。したがって、10 体積の過酸化水素 1.0 mL は、分解すると CNTP 中に 10.0 mL の O 2 を生成します。
過酸化水素の分解は、以下に示す質量と体積の関係を 2 として、次の方程式に従って起こります。 34.02 g の H 2 O 2 は、CNTP で 22.4 リットルの O 2 を生成します。

2H2O2 → 2H2O + O2 ↑
KMnO 4 溶液を H 2 SO 4 で酸性化した過酸化水素溶液に添加すると、起こる反応は次のように考えることができます。
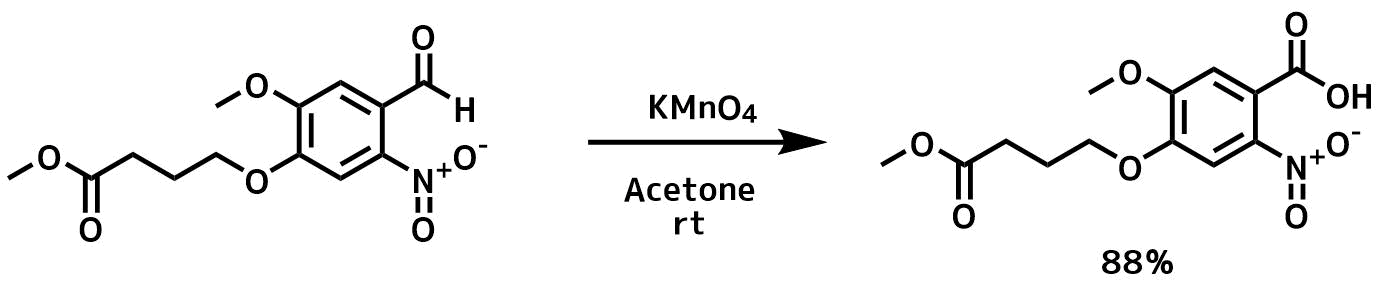
2 KMnO 4 + 3 H 2 SO 4 + 5 H 2 O 2 → K 2 SO 4 + 2 MnSO 4 + 8 H 2 O + 5 O 2 ↑
過酸化水素 (H 2 O 2 ) 含有量の実験室測定は、以下の手順に従って 過マンガン酸カリウム (KMnO 4 ) で滴定することによって行うことができます。
- 研究対象の過酸化水素溶液 (元の溶液) 25.0 mL (または 10.0 mL) を 250.0 mL (または 100 mL) の メスフラスコ (たとえば、10 容量の溶液) に入れます。
- 蒸留水を全量加えて均質化します。このようにして、元の溶液 25.0 または 10.0 mL を含むストック溶液が得られます。
- ストック溶液 10.0 mL をピペットで三角フラスコに移します。この容量には 1.0 mL の元の溶液が含まれています (清潔で乾燥した ピペットを 使用してください)。濡れている場合は、ストック溶液の少量を ビーカー に移し、その部分でピペットを洗います。
- あらかじめ沸騰させた蒸留水 90.0 mL で希釈して、すべての CO 2 を除去します。
- 10.0 mLのH 2 SO 4 を1:5に希釈して加えます。
- 0.1 M KMnO 4 溶液で永久的なピンク色になるまで滴定します。指示は自然です。投与溶液は指標としても機能します。滴定の終点は、投与溶液の色の持続によって示されます。
参考文献:
ルフティ、マンスール。フェラドスとクロマドス:化学知識の社会的生産と私的流用、UNIJUI編、Ijuí/RS – 1992年。
マハン、ブルース・M。ローリー・J・マイヤーズ;化学: 大学コース、Edgard Blucher LTDA、サンパウロ/SP – 2002
ペルッツォ、フランシスコ・ミラガイア(チトー)。カント、エドゥアルド・レイテ。 Chemistry in the Everyday Approach、現代編、vol.1、サンパウロ/SP- 1998。
ギャラリー