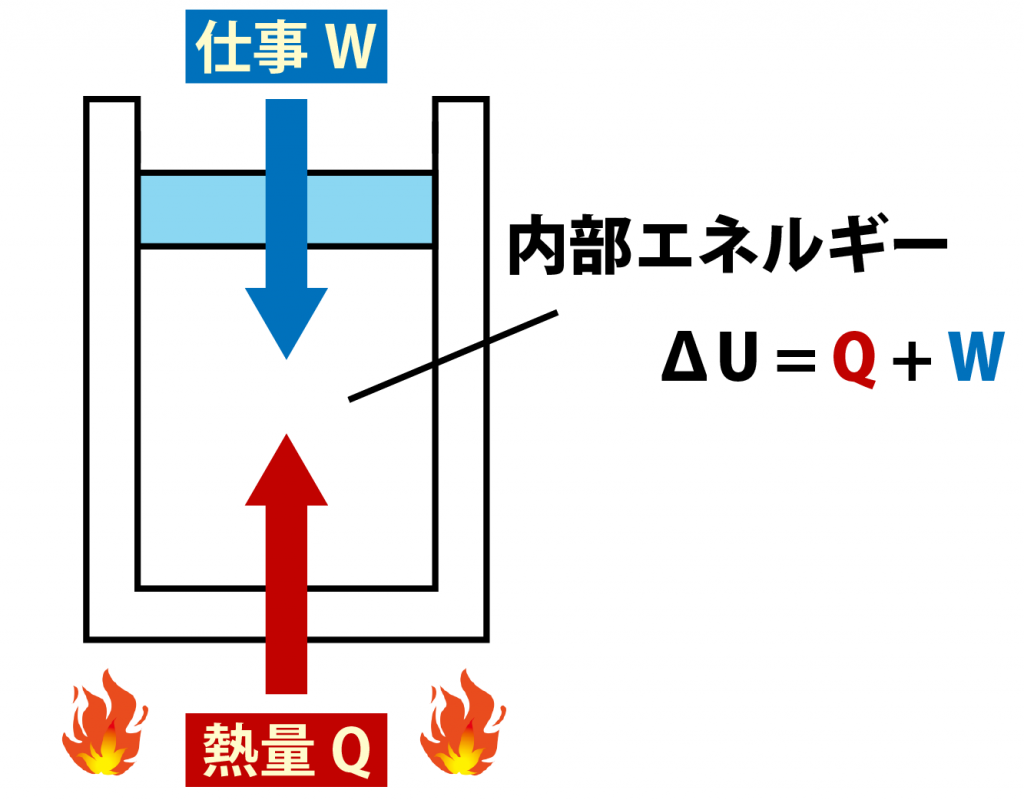
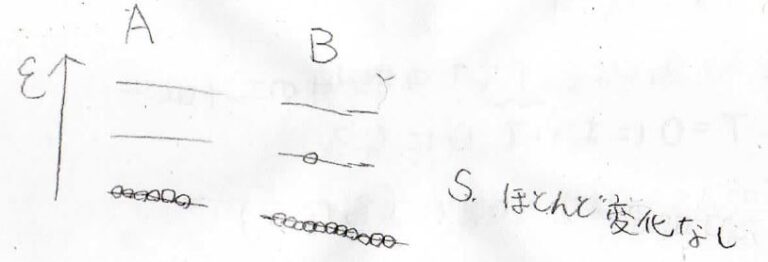熱力学の 3 つの法則 の間には教訓的な比較があります。
- 第 1 法則: 勝つことはできません。
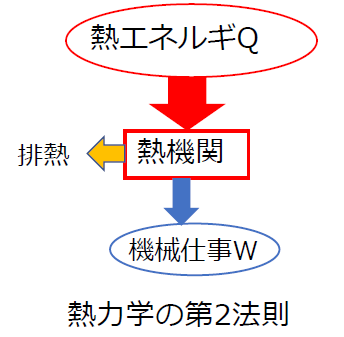
- 第 2 法則: 絵を描くことさえできません。
- 第 3 法則: 絶対零度でのみ描画できます。

言い換えれば、 第 1 法則は 、エネルギーはある形態から別の形態に変化するだけであり、それを作り出すことはできないと定義しているため、「勝てない」という表現が生まれます。 第二法則 は、エネルギーを得る(創造する)ことができないだけでなく、そのすべてを仕事に変えることはできないため、その一部が依然として失われるというもので、そのため「損益分岐点にもならない」という表現が生まれます。
熱力学の第 3 法則 では、絶対零度では機械の効率が 100% になることが可能です。つまり、熱の形での 熱エネルギー は損失なく完全に仕事に変換できます。絶対零度ではエネルギーが生成されないため「引き込み」が発生する可能性があるが、エネルギーは全体的に変換されるため失われることもない、と述べられたのはこのためです。
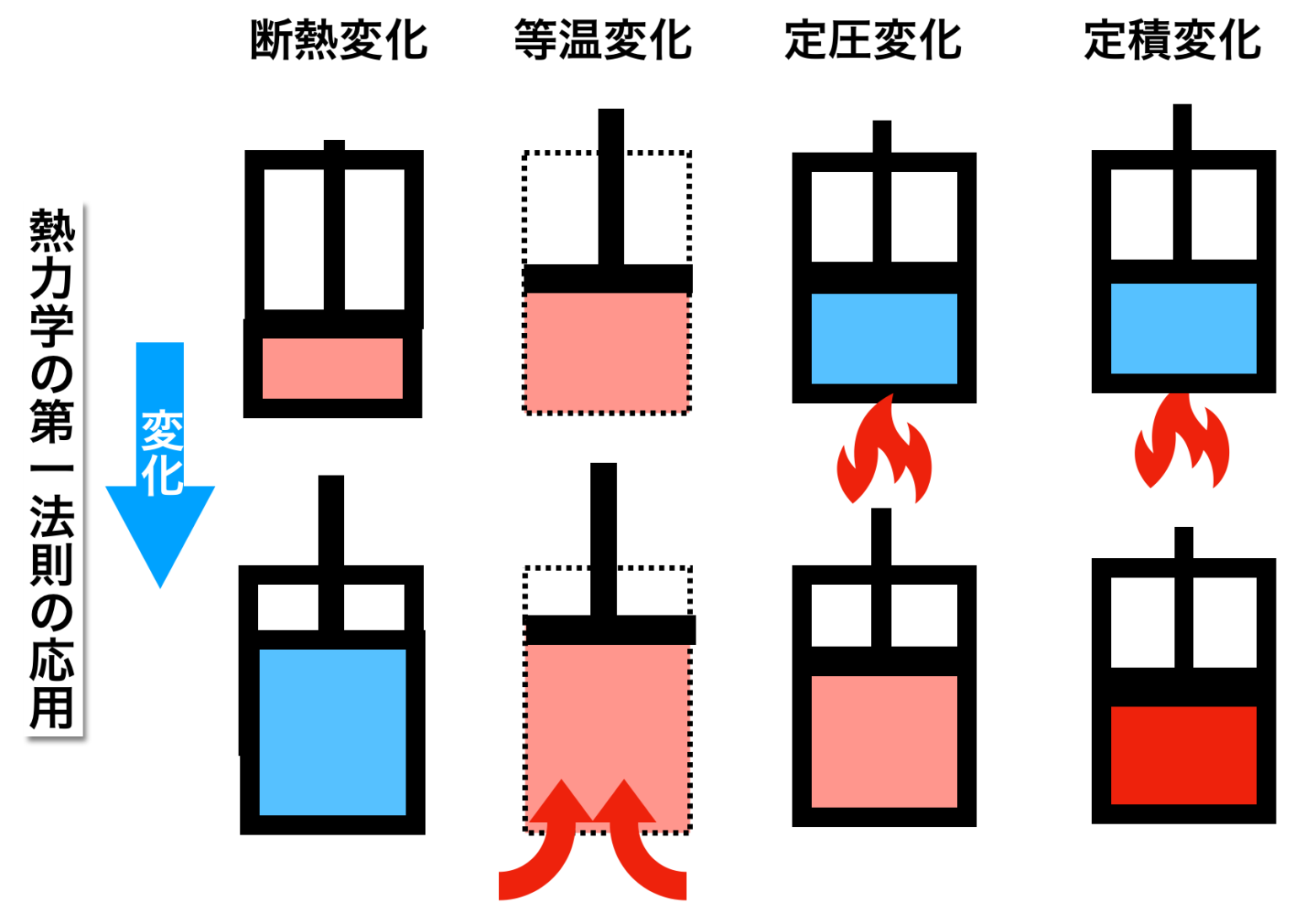
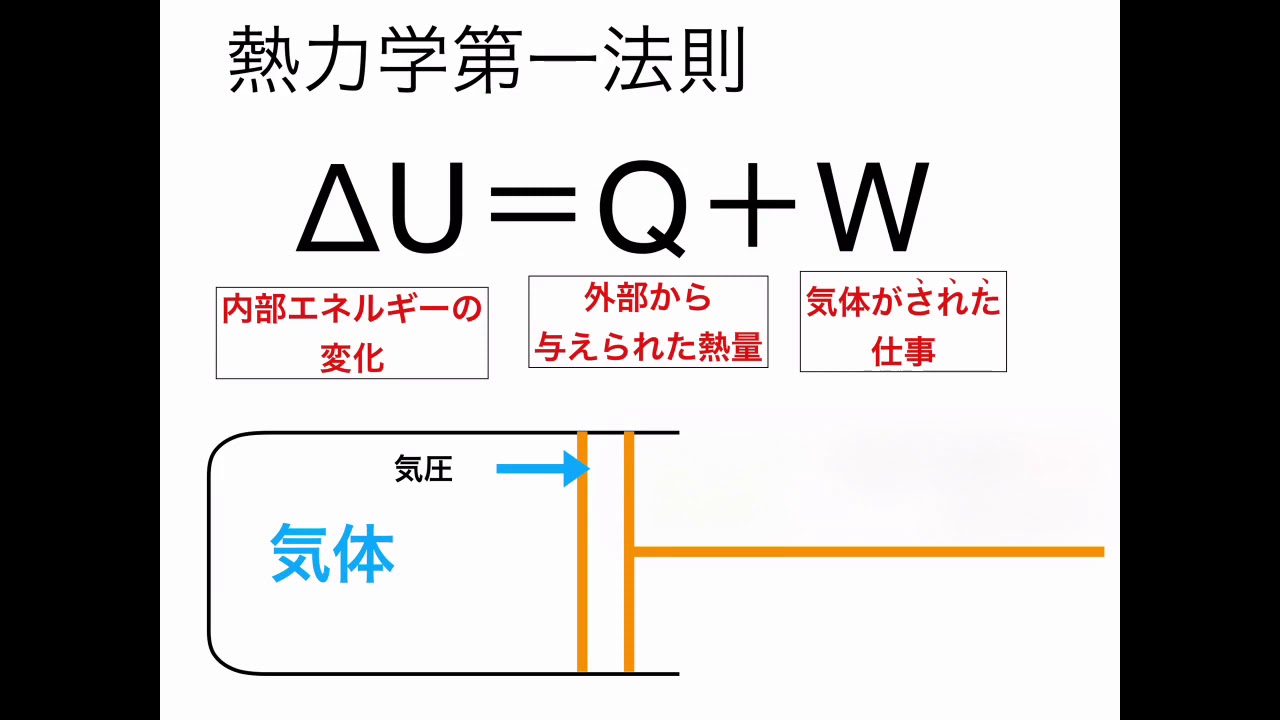
絶対零度では、体の内部エネルギーはゼロであり、分子の運動はありません。 熱力学の第一法則 によると:
ΔU = 0として、
熱は完全に仕事に変わるでしょう。
ただし、実験室では絶対零度に到達したことはありません。つまり、第三法則仮説は、温度が正確にゼロに等しい場合にのみ理論的であることを意味します。ただし、 温度が絶対零度に近づく 状況に関する仮説は排除されませんでした。
1907 年、ヴァルター ネルンスト (1864-1941) は、温度が絶対零度に近づくこれらの状況に対処する法則を提案しました。
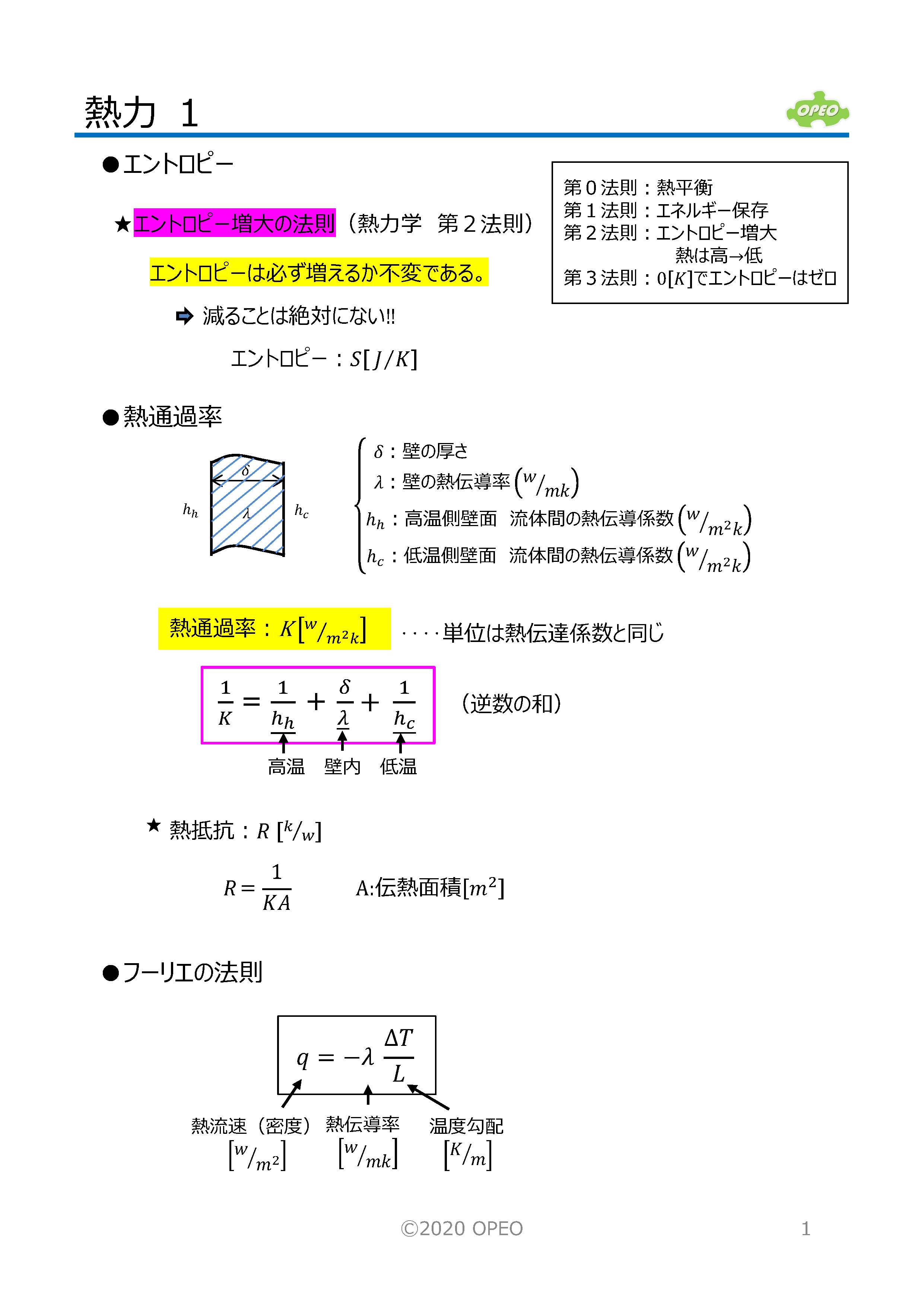
「 温度がゼロになる傾向がある場合、系のエントロピーもゼロになる傾向があります。 」
このネルンストの法則は 、熱力学第 3 法則 として知られるようになりました。
エントロピーは 、システム内の分子の無秩序のレベルを測定します。温度が高くなるほど、加熱された分子がより多く移動し、体積内に広がる傾向があるため、エントロピーは大きくなります。エントロピーの概念を使用すると、 熱力学第 2 法則は 次のように書くこともできます。
「 プロセスが閉鎖系で発生する場合、 エントロピー は決して減少せず、可逆プロセスでは一定のままであり、非可逆プロセスでは増加します。 」

可逆 プロセスは初期状態に戻ることができますが、 非可逆 プロセスは初期状態に戻ることができません。実際の例としては、ホット プレート上に水滴を置くと 加熱されます 。ドロップが初期状態に戻る可能性は低く、このプロセスは不可逆的です。水の入った容器は冷やすと氷になりますが、加熱すると再び液体になります。これは可逆的なプロセスです。
3 つの法則の文脈では、100% の効率を持つ 熱エンジン を実現することは不可能であるため、たとえ η < 1 であっても、 可逆プロセスが 熱エンジンで最大の効率が得られる理想的なプロセスと考えられます。
ギャラリー