遷移元素である 銅は 、わずかに不透明な輝きと心地よい外観を備えた控えめな黄赤色の 金属 で、 周期表 の IB 族に位置し、原子番号 29、原子質量 63.55 g mol です。 、融点 1038°C、沸点 2927°C は、柔らかく、展性があり延性のある金属です。この金属の化学記号はCuで、ラテン語の 「cuprum」 に由来し、初めて発見されたと考えられているキプロス島を暗示しています。

銅鉱石

自然界では主に黄銅鉱 CuFeS 2 の形で存在し、他にもありますが、これは元素状態で存在する金属の 1 つであることに加えて、より高い金属含有量を持っています。

これは、銅が広く使用され始めた 新石器時代 の 青銅器時代 に遡り、知られている中で最も古い金属の 1 つであり、銅の採掘は約 5,000 年前に始まったと研究者は主張しています。この金属は希少であり、その価格が非常に高かった時代がありましたが、その後、頻繁に発見されるようになり、価格は下がりましたが、熱と電気エネルギーを伝導するというその極端な特性が発見され、その使用が普及するようになりました。工業用として価値は大幅に上昇しましたが、貴金属とみなされていたにもかかわらず、 金 や 銀 とは比べものになりませんでした。
その中には次のようなものがあります。
- キッチン用品: ジプシーポット、フライパン、洗面器、カトラリー。
- 電気導体: 高電圧および低電圧ケーブル、コネクタ、電気接点全般、モーター製造。
- 設備:太陽熱ヒーター、熱伝導体 、 水道管 。
- 金属合金: 銅と 錫は 青銅を形成し、銅と 亜鉛は 真鍮 を形成し、最後に銅と金は 18 カラット金を形成します。たとえば、これらは最も一般的で使用される合金ですが、他にも無数にあります。
銅に関する重要な情報
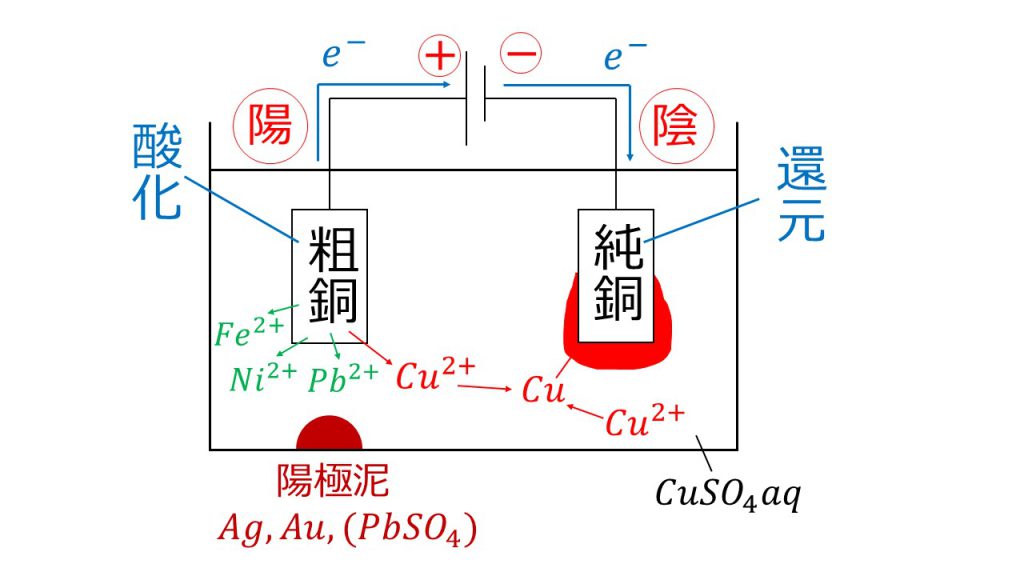
化学的に銅と言えば、いくつかの化合物を形成します。主なものは硫酸銅 CuSO 4 ・ 5H 2 O で、殺藻剤やプールの水に青色を与える剤として使用されます。この塩は無水状態では白色ですが、 吸湿性 があるため、空気に触れると水分を吸収し発色します。金属の精製は、金属が見つかった鉱石を加熱するか、加熱後に 電気分解 を受けてより高い純度を得るという 2 つの方法で行うことができます。銅には 2 つの酸化状態 Cu + と Cu +2 があります。
定性分析では、 水酸化ナトリウム 溶液を添加すると濃い青色のゼラチン状の沈殿が形成されるため、この元素は簡単に識別できます。また、定性分析では Cu +2 のみが重要であることを強調することも重要です。この金属はカチオンの第 2 グループに属し、0.34 ボルトの正の標準電極電位を持っているため、希酸 (HNO 3 、H 2 SO 4 および HCl) による攻撃は不可能ですが、攻撃され、高温の濃H 2 SO 4 に容易に溶解することに加えて、王水にも溶解します。
アルカリ媒体中および 硫酸 と銅の反応:
反応によって上に示した化合物を形成するだけでなく、 配位化合物 も形成します。つまり、アンモニウムや水と錯イオンを形成します。
テトラアミノ銅(II): [Cu(NH 3 ) 4 ] +2
テトラアコ銅酸(II): [Cu(H 2 O) 4 ] +2 (この錯体は銅イオンの水和の結果であり、溶液の濃い青色の原因となります。)
参考文献:
ラッセル、JB
一般化学
。
サンパウロ:マクロンブックス、2004 年。
フォーゲル、アーサー イスラエル、1905 年 – 定性分析化学 / アーサー I. フォーゲル; [アントニオ・ヒメノ・ダ訳]第5版。回転数G. Svehla著 – サンパウロ:メストレ・ジュ、1981年。
マハン、BM 化学: 大学のコース 。第4版サンパウロ:エドガルド・ブリュッヒャー、2003年。
デュワード・シュライバー。アトキンス、ピーター。 無機化学 – 第 4 版。ポルトアレグレ、ブックマン、2008年。
リー、JD。それほど簡潔ではない無機化学 – 第 4 版の英語訳。サンパウロ、エドガルド・ブリュッヒャー、1996年。
https://web.archive.org/web/20110512021709/http://www.ulbra.br:80/mineralogia/colecao/cobre_nativo.htm
ギャラリー