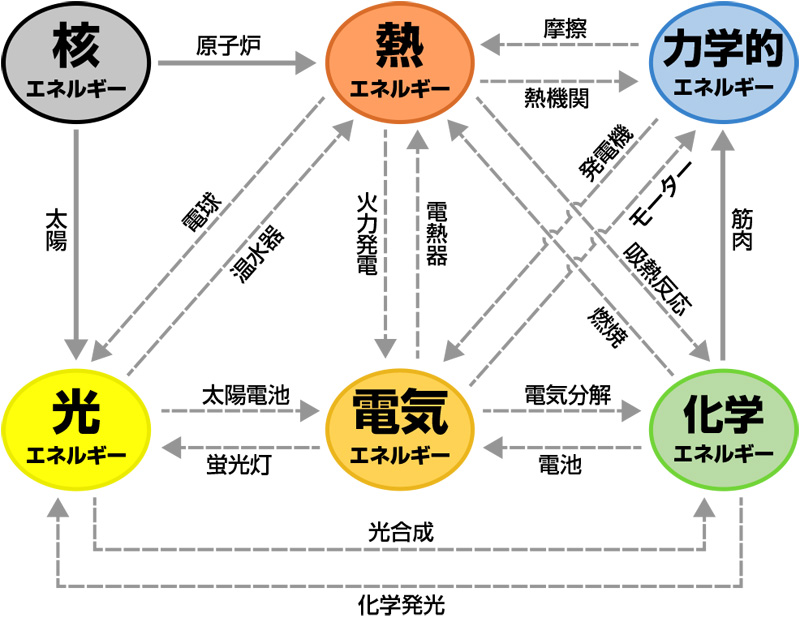
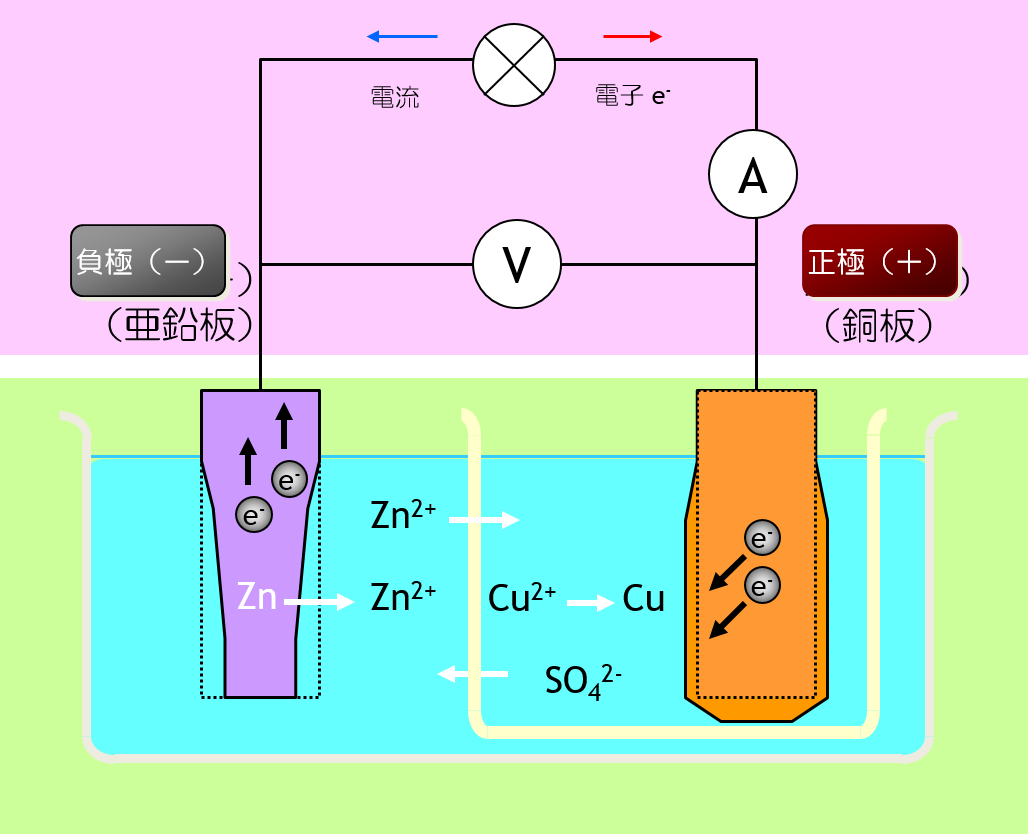
電気化学は 、物質間の 電子 移動を研究する化学の一部です。一部の反応物が電子を失い、他の反応物が電子を獲得して生成物を形成する反応は 、酸化還元または酸化還元反応 と呼ばれます。これらの反応の挙動は電気化学の主要なテーマです。

酸化還元反応では、 酸化 と呼ばれる電子の損失と 還元 と呼ばれる電子の獲得という 2 つの基本的なプロセスが発生します。物質が還元を受けると、結果として別の物質の酸化が引き起こされるため、酸化剤として作用します。同様に、酸化された物質は還元剤として働きます。私たちはしなければならない:
酸化剤 ⇔ 還元を受ける ⇔ 電子を得る

還元剤 ⇔ 酸化を受ける ⇔ 電子を失う
酸化還元反応の特定は必ずしも明らかではありません。一般に、電子移動反応は 細胞や電池 内の反応と関連付けられますが、酸化還元反応は私たちが想像しているよりも一般的です。酸化還元プロセスの例としては、 燃焼 、 呼吸 、 錆など が挙げられます。反応が酸化還元であるかどうかを識別するには、生成物と反応物の 酸化数 (Nox) の変化を評価する必要があります。一般に、酸化数は反応物の各 原子 と生成物の各原子に割り当てられます。変化が発生した場合、電子の移動があったため、反応は酸化還元であると結論付けられます。たとえば、次のような反応を考えてみましょう。

最初のケースでは、単体の酸化数はゼロであり、単核イオンの場合、Nox は電荷に等しくなります。 亜鉛 の Nox は 0 から +2 まで変化し、 水素 の Nox は 0 から +1 まで変化することが分かりました。したがって、それは酸化還元反応です。 2 番目の反応では、すべての原子が一定の酸化数を維持しているため、酸化還元反応ではありません。

つまり、電位差は、還元剤と酸化剤の標準還元電位の差に等しい。標準還元電位は、参照、一般的には 標準水素電極 から得られます。表にされた値を使用して、酸化還元反応の自発性を予測することができます。正の電位差は自発的プロセスを示し、負の電位差は強制または非自発的プロセスを示します。例えば:
最初の反応は、電位がプラスになると自発的に発生します。これはバッテリーまたはボルタ電池の可能性があります。一方、2番目の反応はマイナスの電位を持つため、自然には起こりません。 電気分解 と呼ばれるプロセスで 電流 を供給する必要があります。

参照:
ブラウン、セオドア。ルメイ、H. ユージン。バーステン、ブルース E. 化学: 中心的な科学。 9版プレンティス・ホール、2005 年。
ギャラリー