還元電位の異なる 2 つの物質を適切な条件下で接触させると、自発的な反応が起こります。このタイプのシステムでは、エネルギーが放出され、 電流 の生成に使用できます。この種の反応を使用して電気エネルギーを生成するには、ボル電池またはバッテリーを使用します。

バッテリーの最も重要な特性は、エネルギーを生成する反応が自発的であること、つまり、外部要因の作用なしに反応が起こることです。また、 電気化学 システムに電流の形でエネルギーを供給して、最初は非自発的な反応を強制的に発生させることもできます。この場合、 電気分解 プロセスが発生しますが、これはバッテリーで発生するものとは異なり、発生するシステムへのエネルギーの追加に依存します。電気分解は電池の逆と考えることができます。

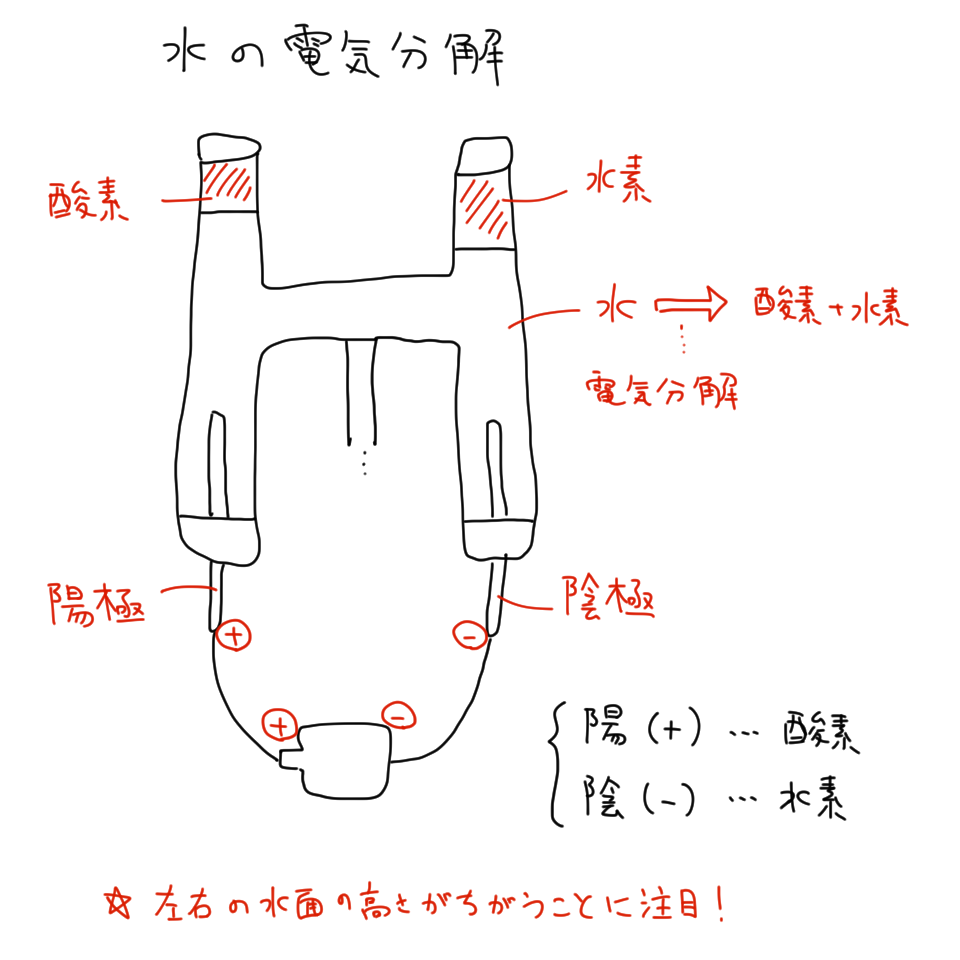
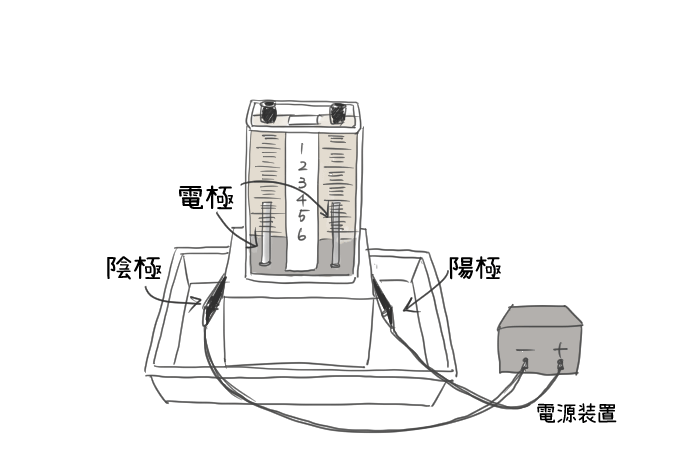
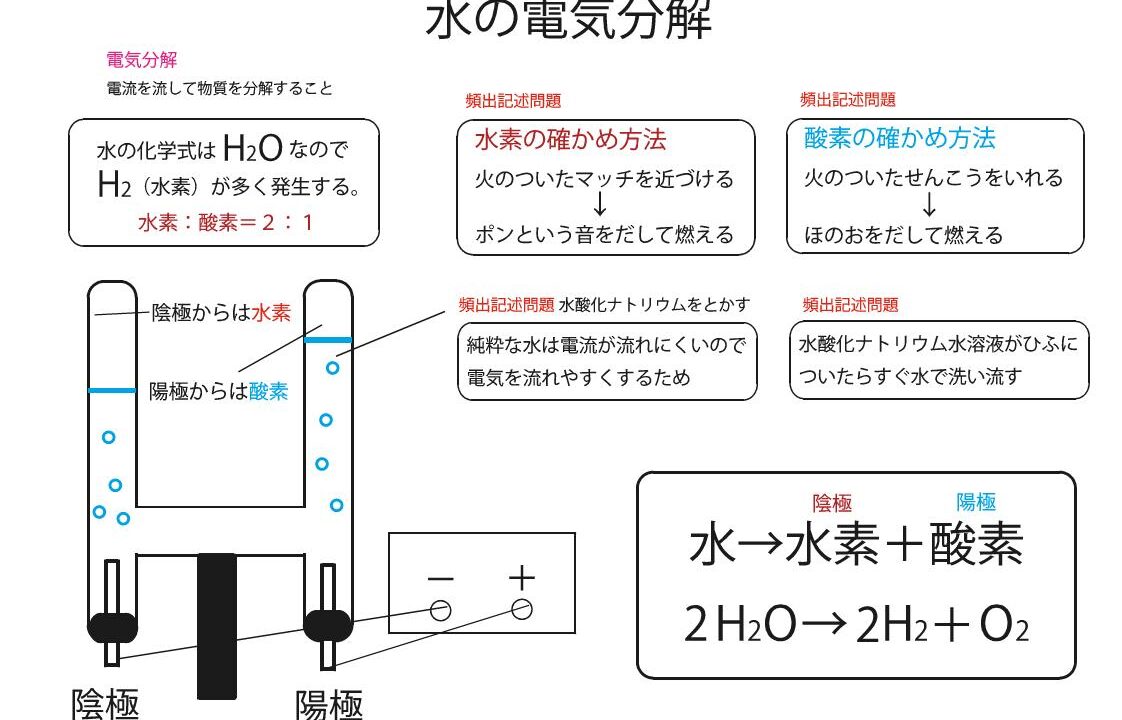
電気分解は有用なプロセスであり、私たちの日常生活に存在しています。たとえば、携帯電話のバッテリーは電池のように機能しますが、充電する際には電気分解が行われます。電気分解には 2 つの最も一般的なタイプがあります。1 つは水溶液中での電気分解で、反応物と生成物が水に浸されて反応に参加します。もう 1 つは 火成電気分解です。火成電気分解 では、電流が溶融固体を通過して目的の生成物が生成されます。 。

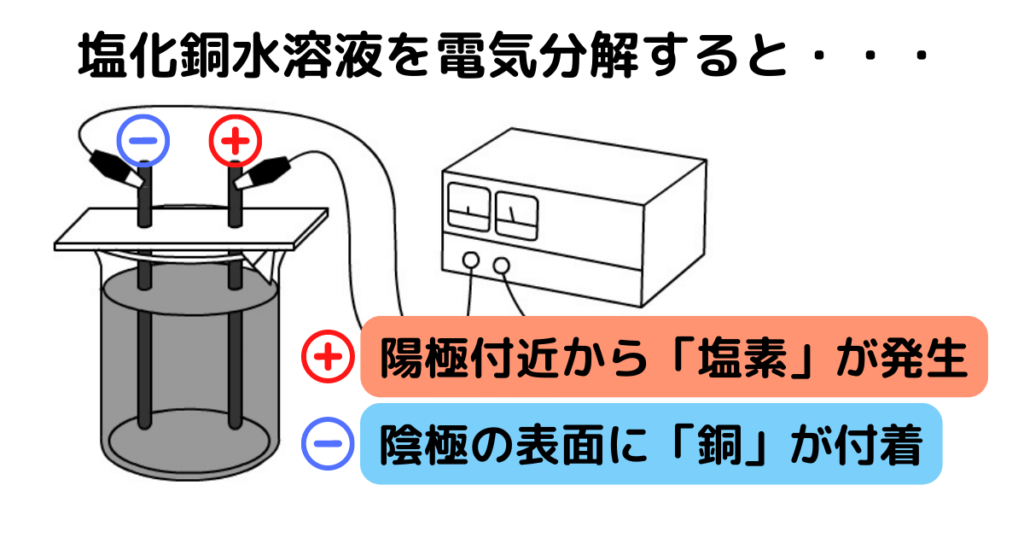
火成電気分解の使用により、電解システム内で水を扱う煩わしさが解消されます。たとえば、 塩化ナトリウム 水溶液中で電気分解を行って金属ナトリウムと塩素ガスを得ることができません。これは、水中の 水素 が還元され、水中の酸素が酸化されるためです。電気分解すると水素と酸素ガスになります。火成電気分解を使用すると、塩化ナトリウムが溶解し、火成液体に電流が流れることで塩素ガスと金属ナトリウムが生成されます。一方、火成法の欠点は、使用する電流だけでなく、固体材料を溶融するのに必要な熱も必要とするエネルギーコストが高いことです。

火成電気分解は塩素および 苛性ソーダ 工業に適用され、溶融塩素塩を電気分解して、水酸化ナトリウム、塩素、 次亜塩素酸ナトリウム 、水素などのさまざまな製品を製造します。金属アルミニウムは火成電気分解によっても生成されます。この場合、溶融氷晶石 (Na 3 AlF 6 ) の浴中で純粋なアルミナ (酸化アルミニウム Al 2 O 3 ) が金属の生成に使用されます。

電気分解プロセスで使用される電極は、プロセスのエネルギー需要に影響を与えるため、非常に重要です。一部の電極は反応に参加し、たとえば消費されます。この場合、電極はアクティブと呼ばれます。そうでない場合、電極は不活性です。還元が起こる電極は、陽イオンがそこに向かって移動するため、陰極と呼ばれます。酸化が起こる電極は、陰イオンがそこに向かって移動するため、アノードと呼ばれます。
参照:
シュレーブ、RN & ブリンク ジュニア、JA – 化学プロセス産業 – 第 4 版グアナバラ・クーガン、SA リオデジャネイロ、1980 年。
ギャラリー