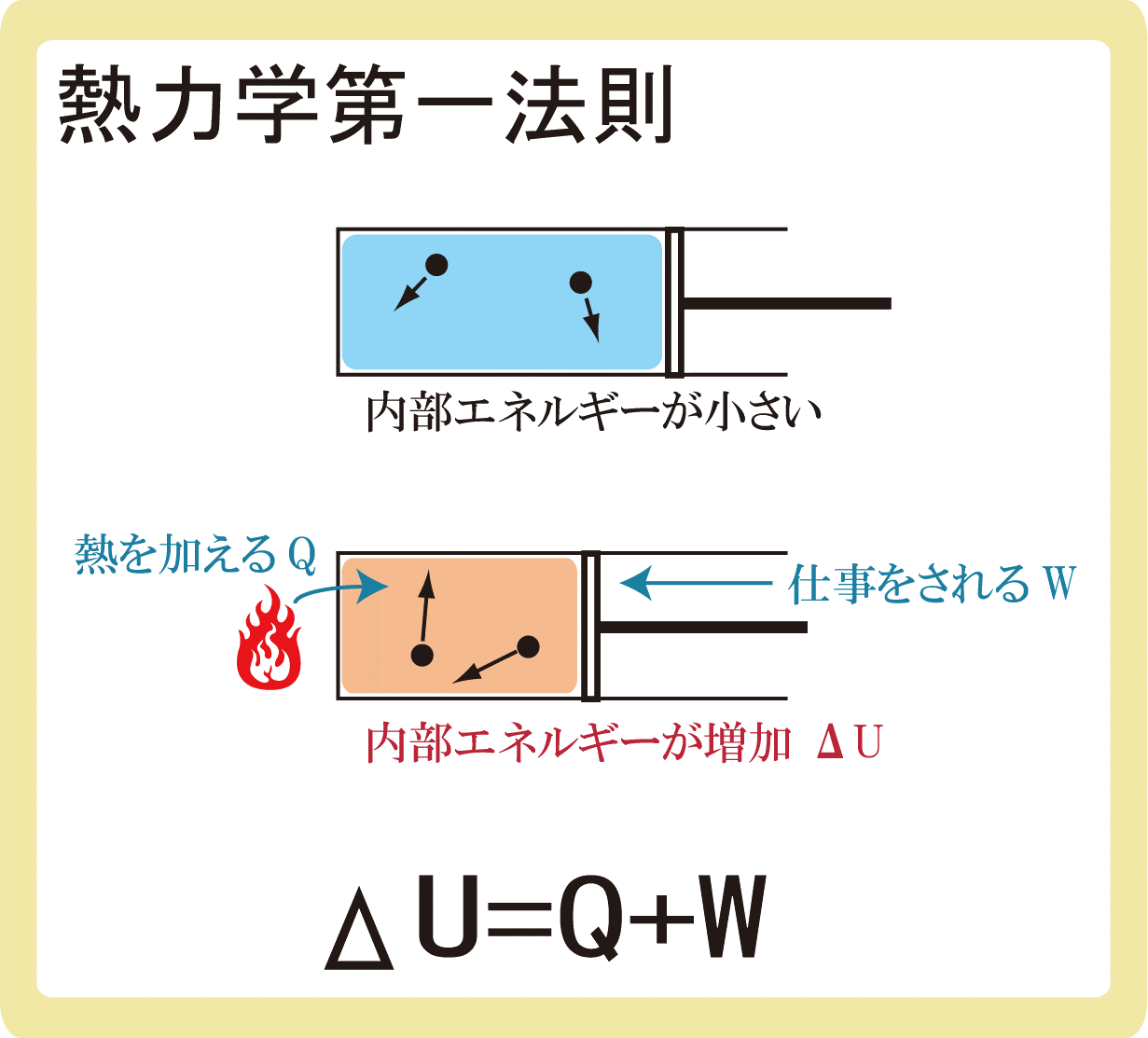
熱力学 という言葉は、ギリシャ語の テルミー (熱)と ダイナミス (力、力)に由来しており、運動中の熱(または移動中の 熱エネルギー )と運動中の 機械エネルギー (仕事)を研究する物理学の分野として定義されています。熱と 温度 の概念を含む現象を扱います。また、システムとその外部環境の間の熱と仕事の交換、これらの交換とシステムの特性間の関係も研究します。
熱力学について語るときは、実行できる 微視的 研究と 巨視的 研究の特徴を強調する必要があります。
熱力学の法則を研究する場合、 顕微鏡での研究を行うことはお勧めできません。これには、膨大な数の粒子 (10 24 のオーダー)、原子、分子が無秩序に動き、互いに衝突することになるからです。そしてそれらを囲むコンテナの壁。
巨視的な記述には、 体積、温度 、 圧力など のパラメータがほとんど含まれず、計算が簡単です。したがって、熱力学の法則の研究では、常に多数の粒子 (2 つや 3 つなどの少数だけでは意味がありません) を含む巨視的な記述が行われ、必要な多くの動きの平均が求められます。ミクロの世界に位置するため、統計的な性質を持ちます。
また、熱力学の法則は、現象学的特徴を備えた経験法則として出現し、その後になって初めて、法則の微視的な研究を提供する統計力学と熱力学が出現したこともわかっています。
この記事の内容
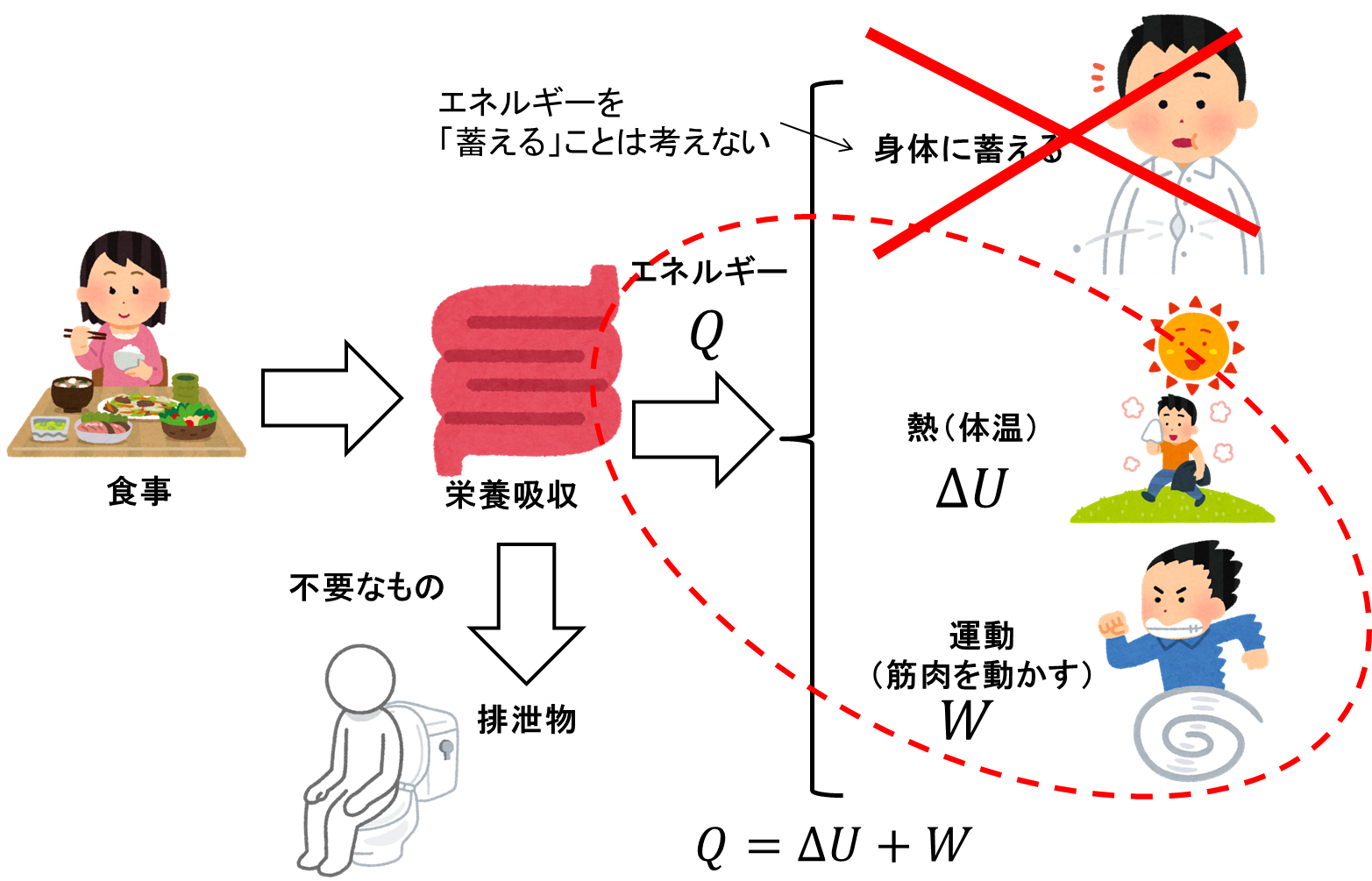
熱力学の第一法則
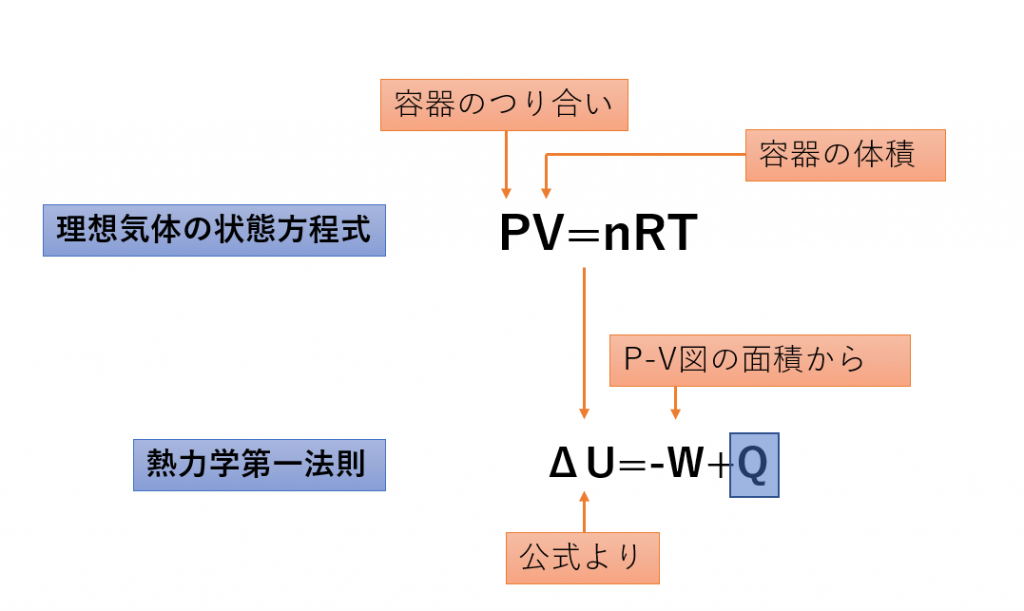
熱力学の第一法則は 、エネルギー保存の原理を定量的な方法で扱います。熱力学プロセスでは、総エネルギーは保存されるため、システムの内部エネルギーの変化 (ΔU) は、環境と交換される熱 (Q) と周囲のシステムによって実行される仕事 (τ) の差になります。力の:
つまり、システムはエネルギーを生成したり破壊したりすることはできず、エネルギーを変換するだけです。

熱力学の第二法則
熱力学第 2 法則は、 熱力学プロセスの 定性分析を 行います。
それには クラウジウス の 2 つの声明があり、次のように結論付けられています。
低温源から高温源に熱を伝達するだけのシステムは不可能であり、あるいはシステムにエネルギーを提供する低温源から高温源に熱を移動することのみが可能です。
そして、 ケルビン の声明は、要約すると次のようになります。
循環変換では、単一の熱源から受け取ったすべての熱エネルギー (熱) を機械エネルギー (仕事) に変換することは不可能です。
つまり、仕事がない限り、冷たい体から熱い体へ熱が流れることはありません。そして、サイクルで作動する 熱機関 では、すべての熱が仕事に変換されるわけではなく、一部は失われます。
第 2 法則は依然として、エントロピーが一方向にのみ変化する可能性があることに注意して定義されています。
エントロピーは、システムの不可逆性 (無組織化) のレベルを測定する 宇宙 の特性です。エントロピーが大きいほど、不可逆性も大きくなります。絶対零度では組織の乱れはありません。
第二法則は、宇宙の エントロピーは 常に増加し、絶対零度には決して到達できないことを証明しています。

熱力学の第三法則
熱力学第 3 法則は 、最小値が 絶対零度 である絶対温度スケールで、このスケールの最小値ではすべての物質のエントロピーが同じであると定義します。
熱力学の第ゼロ法則
熱力学の第 0 法則は、 最初の法則の後に導入されました。これは、最初の法則の後に完成したため発生しましたが、それらの基礎となるものであったため、他の法律より先に来るために、それはゼロ法と呼ばれました。
この法則は、2 つの系が 3 番目の系と熱平衡にある場合、これら 2 つの系は互いに熱平衡にあると定義しています。たとえば、温度計の場合はこれと同じことが起こります。 2 つの物体の温度が同じかどうかを調べるには、 温度 計で両方の物体を測定するだけです。同じマークがある場合、それらは互いに熱平衡状態にあります。
熱平衡とは温度が等しいことを思い出してください。
参考文献:
NUSSENZVEIG、Moysés、基礎物理学コース: 流体、振動、波、熱 – Vol. 2、4 ed。 – エドガルド・ブリュッヒャー、2002年。
ギャラリー