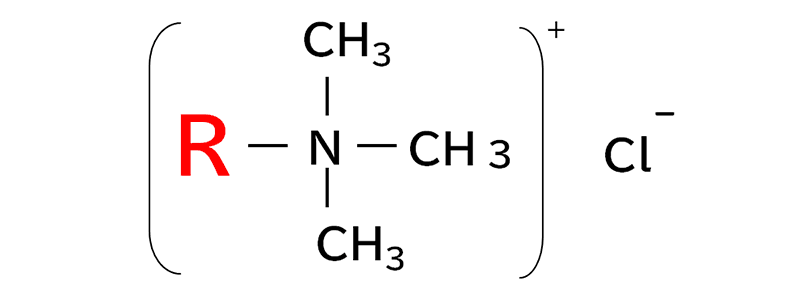
界面活性剤化合物 または 界面活性剤 は有機物質であり、その主な特徴は 両親媒性 の挙動を示すこと、つまり、 極性物質と非極性物質 の両方と相互作用できることです。この特性は、これらの分子が疎水性領域と親水性領域を持っているという事実によって説明されます。 炭素鎖 である疎水性部分は非極性物質と相互作用し、親水性またはイオン性部分は極性物質と相互作用します。
界面活性剤の有機構造を以下に図示します。

図 1: 界面活性剤の有機構造の図。
界面活性剤の相互作用は、界面活性剤が形成される鎖のサイズと環境に対する親和性に関係します。
これらの化合物は、アニオン性、カチオン性、非イオン性、または両性界面活性剤として分類できます。アニオン酸は水に溶解すると解離し、炭素鎖がアニオンを形成します。このタイプの界面活性剤の例としては、シャンプーに広く使用されているラウリル硫酸ナトリウムまたは ドデシル 硫酸ナトリウムが挙げられます。
H 3 C- H 2 C- H 2 C- H 2 C- H 2 C- H 2 C- H 2 C- H 2 C- H 2 C- H 2 C- H 2 C- H 2 C-OSO 3 で ⇒
H 3 C- H 2 C- H 2 C- H 2 C- H 2 C- H 2 C- H 2 C- H 2 C- H 2 C- H 2 C- H 2 C- H 2 C-OSO 3 – + ナ +
図 2: 水中でのラウリルの解離を表す反応
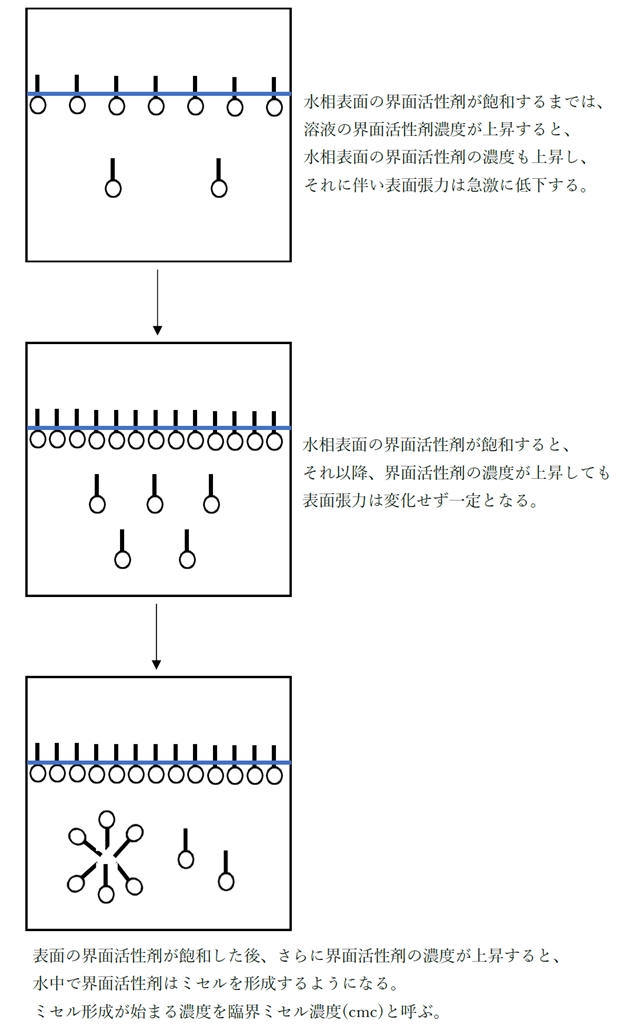
シャンプーの機能は界面活性剤化合物の挙動を明確に示しており、髪の洗浄は次のように説明されます。 分子 の疎水性部分は汚れやグリースと相互作用し、極性部分は水と相互作用して、球状ミセルを形成し、そこで汚れが集中します。髪の内側と静電気の力によって水分が外側に保たれるため、髪をすすぐとミセルが引きずられて汚れが取り除かれます。食器用 洗剤 や石鹸の働きも同様です。

図 3: ミセル。イラスト: DariaRen / Shutterstock.com
カチオン性界面活性剤の場合、水に溶解すると炭素鎖がカチオンを形成します。一例は、コンディショナーや抗菌溶液に含まれる第四級アンモニウムのハロゲン化塩です。非イオン界面活性剤は環境に影響を与える電荷を持たないため、水に溶解してもイオン化しません。例として、ノニルフェノール、 アミド 、エトキシル化 脂肪酸 を挙げることができます。両性界面活性剤は、同一鎖内に カルボキシル 基と第四級アンモニウム基を有するため、溶液のpHに応じてカチオン性およびアニオン性の挙動を示します。この特性により、泡安定剤、洗浄剤、皮膚軟化剤として化粧品業界で広く使用されています。
界面活性剤の両親媒性挙動により、異なる極性の媒体間で相互作用する能力が得られ、 表面張力を 低下させる能力があるため、不混和相の調停剤として使用できます。この特性により、 エマルション 、泡、懸濁液、マイクロエマルションの形成が可能になり、液膜の形成、表面の湿潤化、洗浄にも使用できます。界面活性剤の主な用途としては、これまでに挙げた用途以外にも、農薬、塗料、食品、医薬品、潤滑油などの製造があります。
参考文献:
アトキンス、P.W.ジョーンズ、ロレッタ。化学の原理: 現代生活と 環境 を問う、単巻。第3版ポルトアレグレ:ブックマン、2006年。
ティトとカント。日常的なアプローチにおける化学。 1 冊、パート B – 物理化学。編集者サライバ、2005 年。
ソロモンズ、TWG、フライル、CB 有機化学。第 1 巻、7 編リオデジャネイロ、LTC、2001 年。
Daltin, D. 界面活性剤: 化学、特性、および用途。サンパウロ、エドガー・ブランチ編集部、2012 年。
ギャラリー