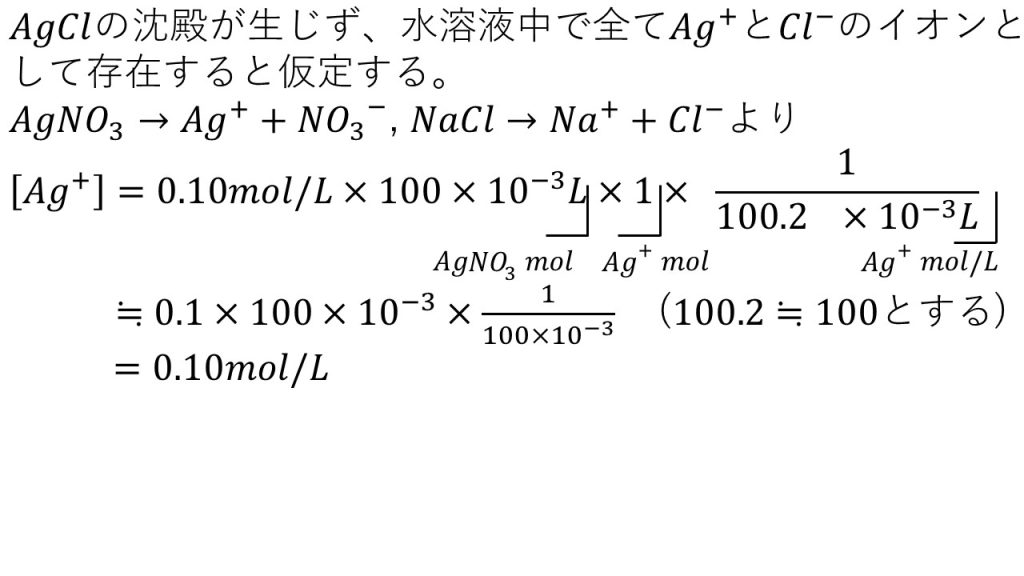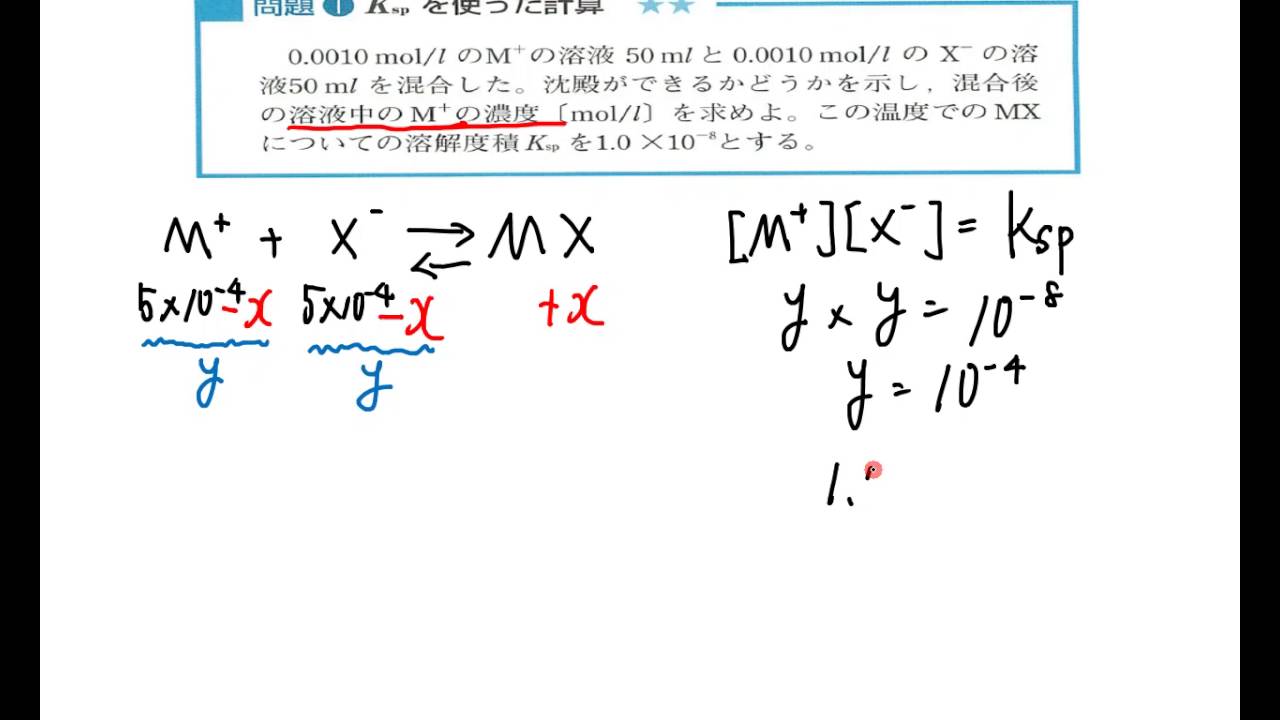任意の電解質 AaBb を使用すると、その イオン解離は 次のようになります。

AaBb <–> aA +b + bB -a
「 溶解度積は 、飽和溶液中に存在する イオン の濃度(mol/L)の積であり、各濃度はイオン解離方程式のイオン係数に引き上げられます。」
言い換えれば、上記のイオン解離方程式に従うと、次のようになります。

Kps = [A +b ] a 。 [B -a ] b
kps 値は、特定の温度では各物質で一定です。いくつかの例を見てみましょう。

水溶液中、25℃、
1 – CaF 2 <–> Ca +2 + 2F – 、Kps = [Ca +2 ]。 [F – ] 2 = 4.9 × 10 -11

2 – FeS <–> Fe +2 + S -2 、Kps = [Fe +2 ] 。 [S -2 ] = 5 × 10 -18
以下に、いくつかの一般的な物質の Kps 値の表を示します。
| 名前 | 式 | 溶解度積 (Kps) |
|---|---|---|
| 硫酸カルシウム | ケース 4 | 9×10 -6 |
| 水酸化カルシウム | Ca(OH) 2 | 4× 10-6 |
| オルトリン酸カルシウム | Ca 3 (PO 4 ) 2 | 2× 10-29 |
| 硫酸 バリウム | BaSO4 | 1×10 -10 |
| 水酸化 アルミニウム | Al(OH) 3 | 1× 10-33 |
| 硫化カドミウム | CD | 8×10 -27 |

以下の点に留意することが重要です。
Kps 値は、難溶性電解質の飽和溶液中でのみ一定のままです。
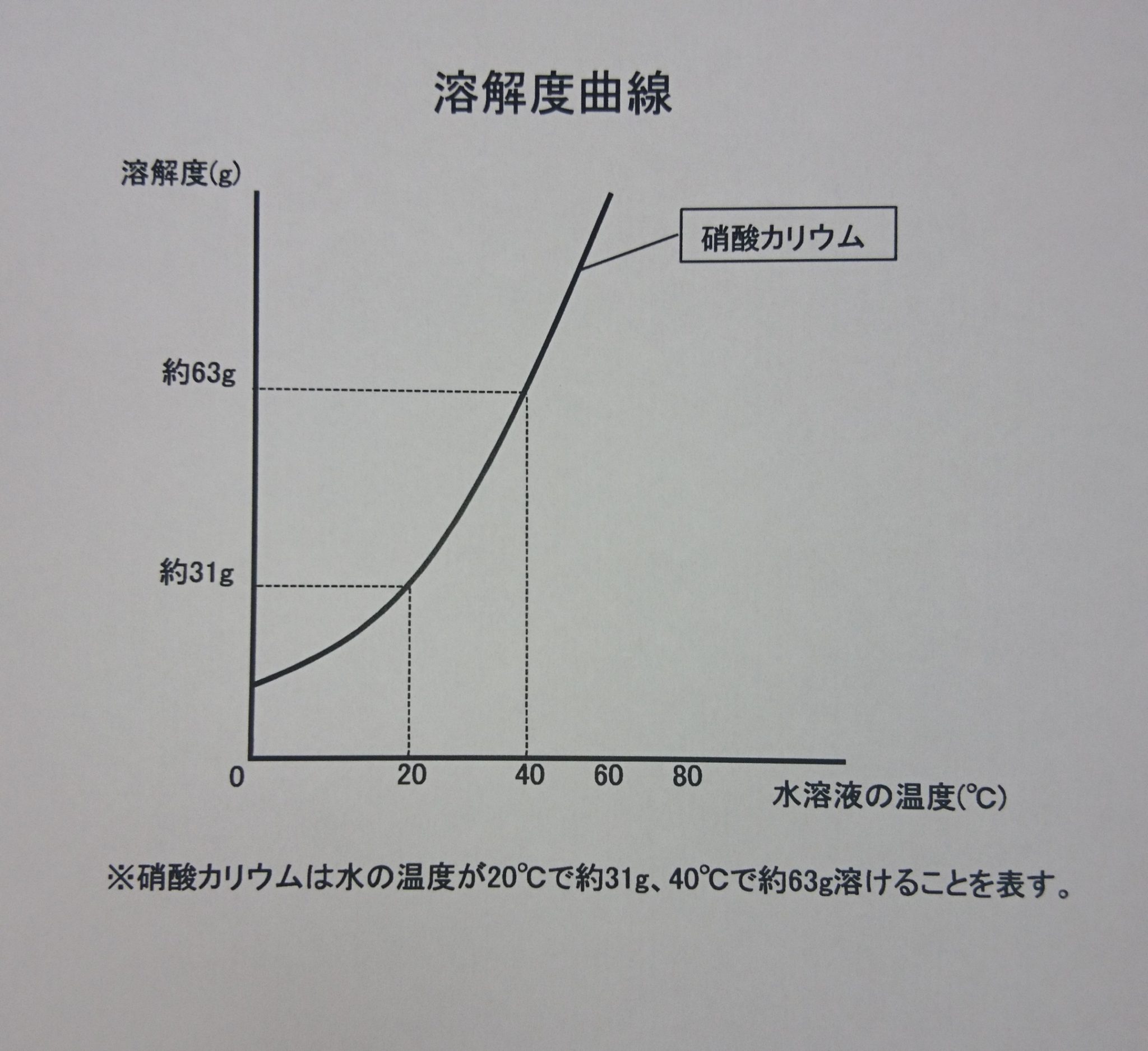
イオン解離が 吸熱性 である場合、温度を上げると溶解度が増加するため、Kps 値は増加します。溶解が 発熱性である場合、 上記とは逆のことが起こります。したがって、温度によって Kps の値が変化すると結論付けることができます。
こちらもお読みください:
ギャラリー