海洋は 地球の表面の 3/4 を覆っており、いくつかの地球規模の気候プロセスにおいて決定的な役割を果たしています。たとえば、地球の温度の維持は、この 生態系 に関連する主要な現象の 1 つであり、 大気 から 二酸化炭素 を吸収し、海底に移動させる役割を果たしています。しかし、大気中へのCO 2 の過剰な排出によって引き起こされる大気と海洋のシステムの不均衡は、海洋のpHの変化を引き起こし、水生動植物に深刻な影響を与えています。 海洋酸性化 と呼ばれるこの現象は、pHの低下で構成されており、これにより、さまざまな海洋動物の代表的な骨格や殻を作るために使用される物質で ある炭酸カルシウム の補償深さが変化します。
この記事の内容

海洋によるCO 2 の回収
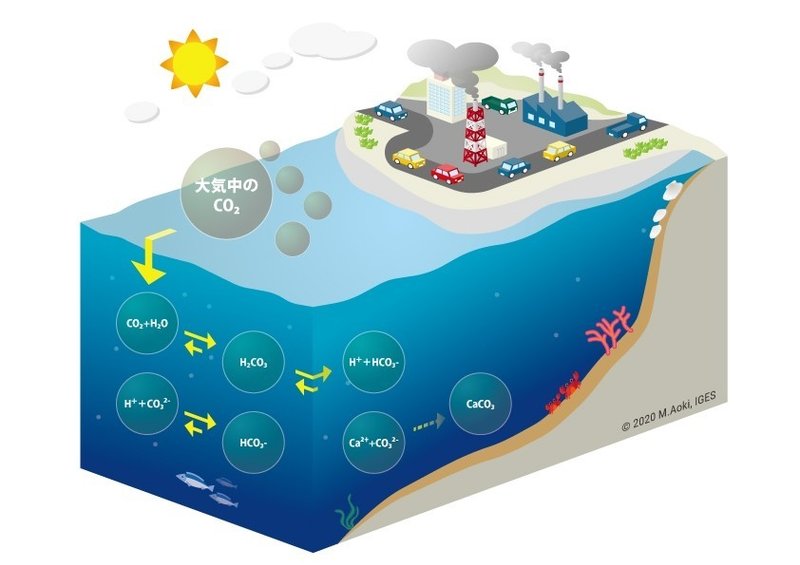
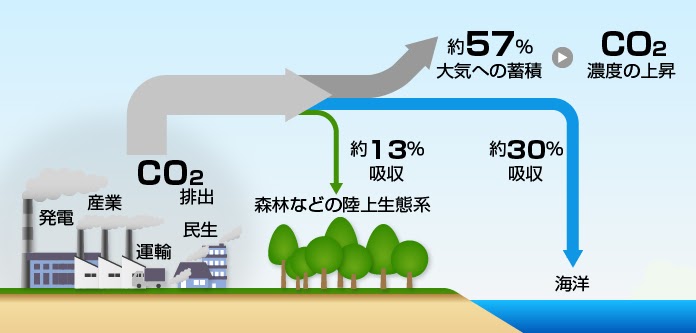
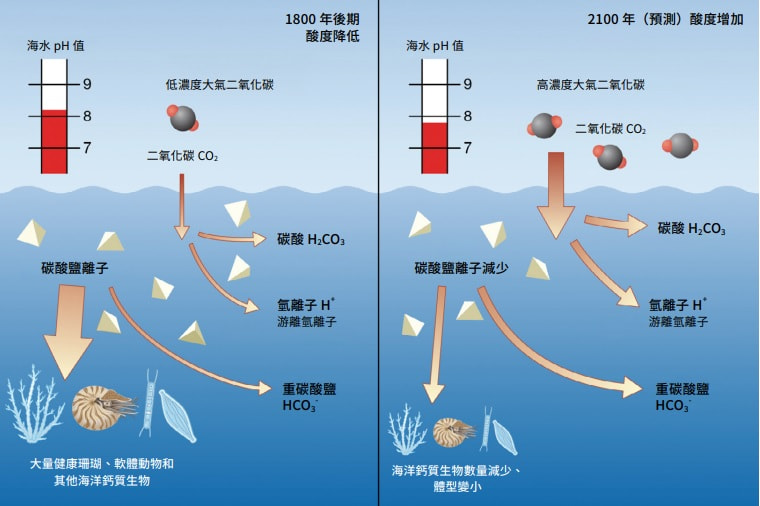
大気中に存在する二酸化炭素の約 1/3 は海洋に吸収されます。水生環境では、この分子は一連の化学変化を経て、その元素が再結合して新しい化合物を生成します。まず、二酸化炭素が水と混合し、水性 CO 2 と 炭酸 (H 2 CO 3 ) が生成されます。この化合物は 弱酸 として分類され、すぐに解離して重炭酸イオン (HCO 3 – ) と H + を生成し、水生環境に存在する他の 分子 と反応します。重炭酸イオンは化学反応も起こして炭酸イオン (CO 3 2- ) に変化し、水柱 (H + ) に 水素 を放出します。このように、炭酸とそれに続く化合物の形成は海洋の pH 低下に大きく寄与し、環境に酸性度を与えます。ただし、このプロセスは通常、海洋で完全に起こるわけではなく、海洋には pH の急激な低下を回避するメカニズムがあるためです。平衡状態を形成する傾向により、重炭酸イオン (HCO 3 – ) を炭酸塩 (CO 3 2- ) に変換することが困難になり、水柱中に放出される H + イオンの量が制限されます。さらに、水性媒体中の過剰な H + イオンも 化学反応を逆方向にシフトさせ 、媒体のバランスを回復するためにこれらのイオンを利用可能な炭酸塩分子 (CO 3 2- ) に結合させる可能性があります。
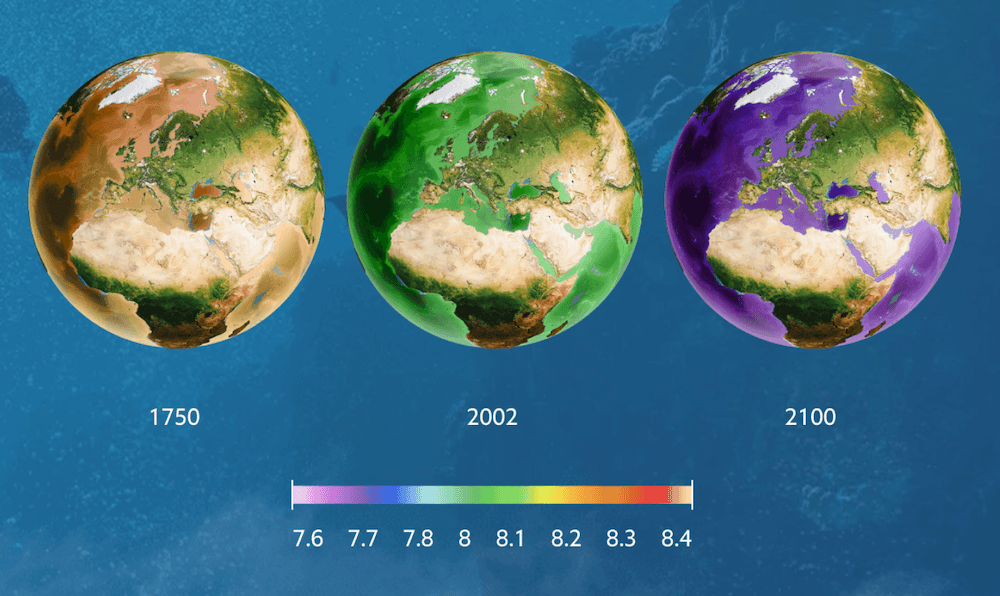
CO 2 水溶液、重炭酸塩 (HCO 3 – ) および炭酸塩 (CO 3 2- ) の濃度の合計は、海洋に溶解している無機炭素の総量を表します。ただし、これらの形態は、水の pH に応じて、多かれ少なかれ優勢になることが交互に起こります。現在、海に溶解している炭素の 90% は重炭酸塩 (HCO 3 – ) の形で表され、海洋の pH は約 8.1 です。炭酸塩は海洋環境で 2 番目に多く利用可能な形態 (10%) ですが、炭酸 (H 2 CO 3 ) と結合した水性 CO 2 は、海洋に溶解している無機炭素の 1% 未満に相当します。しかし、水柱への CO 2 の継続的な添加は pH の低下をもたらし、炭酸形態間のバランスに影響を及ぼします。水性 CO 2 と重炭酸塩 (HCO 3 – ) の濃度はおそらく上昇し、炭酸塩 (CO 3 – ) のレベルは上昇します。 2- ) は過剰な H + イオンとの結合により崩壊します。このような変化は、CO 2 排出量の増加によって引き起こされる、海洋酸性化に対する人間の影響の主な証拠を表しています。

過剰な 二酸化炭素 と海洋酸性化

業界は毎年、何百万トンもの汚染物質を大気中に放出しています。写真:タチアナ・グロゼツカヤ/Shutterstock.com
海洋の酸性化は 産業革命 によって始まりました。それ以来、海の酸性度は 30% 増加しました。この現象は少なくとも 4,000 万年間記録されていません。産業時代の始まり以来、海洋は大気から約 5,250 億トンの CO2 を吸収しており、その量は 1 日あたり 2,200 万トンに達します。 化石燃料 、石油、ガスの燃焼によって生成される過剰な CO 2 は 、大気の変化 (例: 大気汚染 、 温室効果 ) や海洋 (例: 酸性化) を通じて気候に影響を与える結果を引き起こしています。記録によると、産業革命の初め以来、海洋の pH は 8.2 から 8.1 に低下しており、その低下は今世紀末までに最大 0.4 pH 単位増加する可能性があります。これらの値は重要ではないようですが、pH は 対数スケール で測定されることを覚えておくことが重要です。つまり、その効果は単位ごとに 10 倍になります (例: pH=5 は pH=5 の 10 倍酸性です)。 6、および pH=7 の 100 倍酸性です)。したがって、pH を約 7.7 の値に下げると、水は最大 120% 酸性になります。これは、海洋生態系と、生存を確保するために海に依存している何十億もの人々に深刻な影響をもたらすでしょう。
主な影響
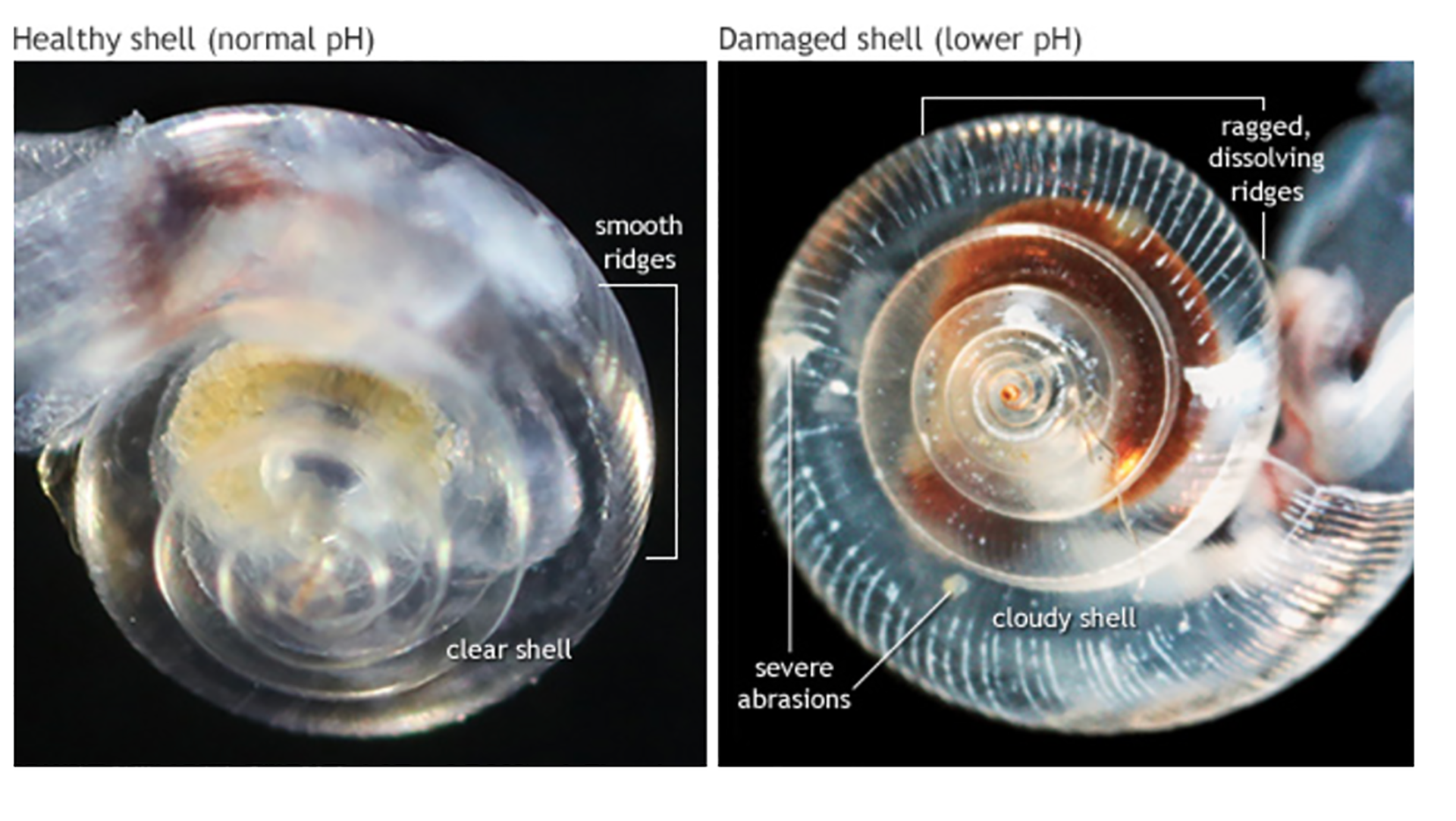
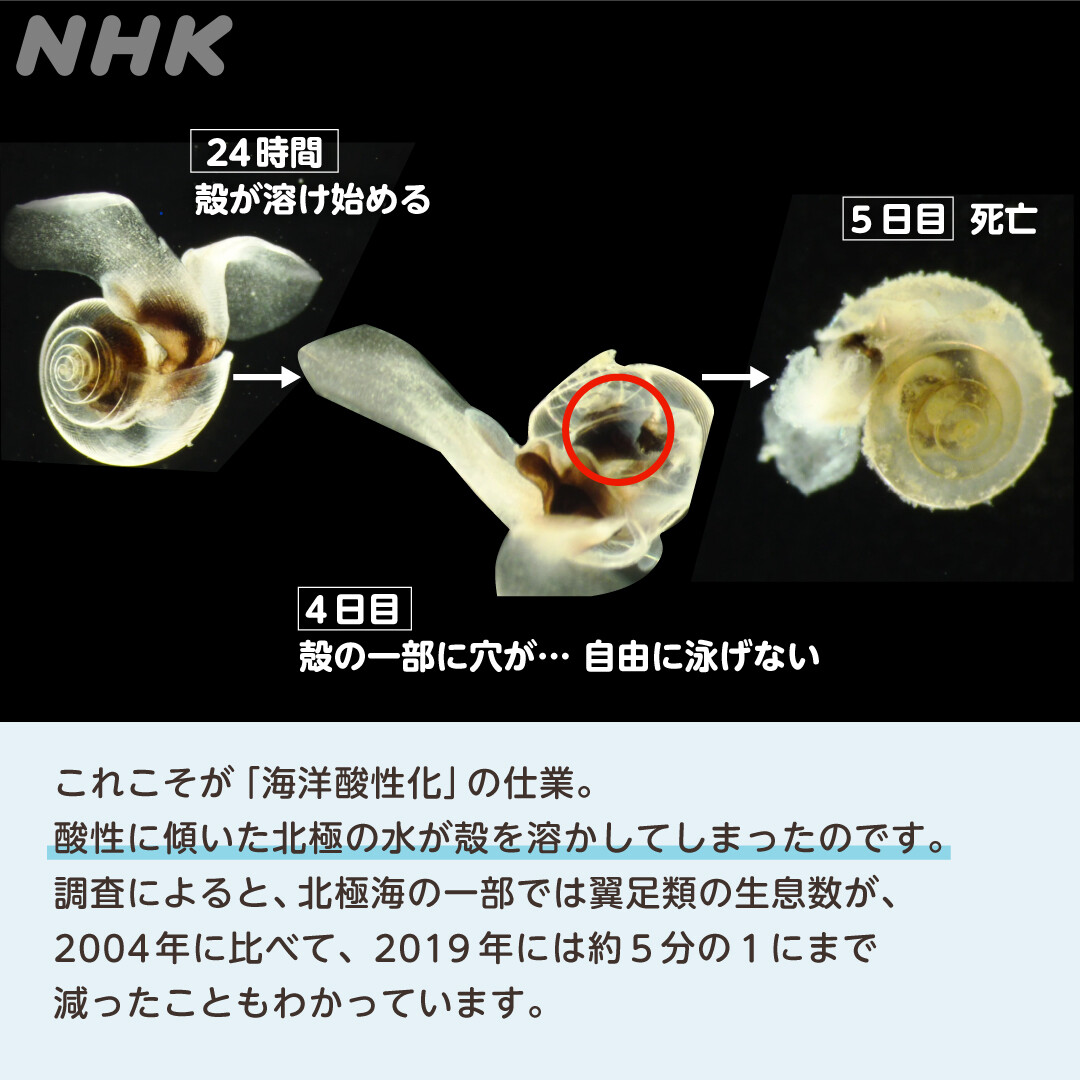
海洋の pH の急激な変化は、海洋動植物に大きな影響を与えます。この現象に関連する最も憂慮すべき影響の 1 つは、リゾクリン層の深さの変化です。この層は、炭酸塩の補償が起こる海洋深度、つまり炭酸塩 (CO 3 2- ) が水柱に溶解する深さに対応し、この化合物によって形成された構造 (殻や骨格など) を維持できなくなります。
一般に、リゾクリンは深さ 4 km に位置しますが、圧力、温度、水生環境の酸性度の変化に応じて変動します。 pH との関係では、CO 2 の濃度が高くなるほど (媒体が酸性になるほど)、炭酸塩 (CO 3 2- ) の安定性が低下し、 カルシウム などの他の化学元素と結合することが困難になります。これは、炭酸塩 (CO 3 2- ) がカルシウム (Ca) よりも H + イオンとの化学親和性が高いために起こります。したがって、酸性環境(H + の利用可能性が高い)では、H + イオンを中和して pH のバランスをとるために、炭酸塩 (CO 3 2- ) がカルシウム (Ca) から解離して水素 (H + ) と結合する傾向があります。媒体の。したがって、水生環境中の過剰なCO 2 は リゾクリンの深さの減少を引き起こし(この層はより浅い深さに移動します)、その結果、体の組成が炭酸カルシウムに依存するいくつかの生物の生息環境が抑制されます。海洋動物( 軟体動物 、 動物プランクトン生物 および 植物プランクトン 生物、サンゴ藻など)の殻や骨格などの構造物は、リソクリンの深さの変化によりすでに溶解しつつあります。海洋の酸性化は、新しいサンゴ礁の建設を制限するだけでなく、既存の サンゴ礁 の腐食も引き起こしています。行動の変化も、海洋生物の酸性化の結果の 1 つである可能性があります。成長の低下、性的成熟の遅れ、聴覚、視覚、平衡感覚などの感覚の低下などは、アシドーシスを避けるために体内のpHバランスを維持するために代謝エネルギーを使用することによって影響を受ける可能性のあるプロセスの一部です。 (魚など)。

サンゴ礁。写真: Andrey_Kuzmin / Shutterstock.com
要約すると、海洋酸性化は 生物多様性 の損失を引き起こし、いくつかの動物群に影響を与え、魚や 水産養殖 に関連する食料生産に影響を与えます。このように、この気象現象は何百万もの人々の食糧安全保障を脅かしており、観光産業や海洋環境に関連するその他の活動から得られる可能性のある利益にも影響を与えています。
参考文献:
海洋生物学。ペレイラ、RC、ソアレスゴメス、A. (2002)。
リオデジャネイロ: Interciência、2、608。
オーシャンポータル – あなたの青を見つけてください。スミソニアン国立自然史博物館。 http://ocean.si.edu/ocean-acidification
ナショナル ジオグラフィック: 海洋酸性化。 http://www.nationalgeographic.com/environment/oceans/critical-issues-ocean-acidification/
ギャラリー