化学元素の塩素は 、塩化物 イオンの 形で NOX -1 を生成し、このようにして、正の性質を持つ多数の元素と化学的に結合することができます。分子内に存在する カチオン の中に 水素 が存在すると、 酸 が生じます。このタイプの化合物の主な例は、その特性と産業および研究室の両方への応用性に関して、塩素金酸、塩素酸、塩酸、および亜塩素酸です。
主な塩素酸
- 塩化金酸 : 塩酸 (HCl) の存在下で、塩化 金 (AuCl) は分子式 HAuCl 4 の塩化金酸を生成します。この酸は、実験室で金が王水に溶解されるときにも生成されます。加熱すると、HCl が分解して放出され、金塩 (塩化物) に戻ります。
- 塩素酸 : 塩素元素に由来する酸素酸で、分子式は HCIO 3 です。 最大濃度 40% の水溶液中にのみ存在します。これは不安定で、穏やかな温度で式 3HCIO 3 -> HCIO 4 + 2CIO 2 + H 2 O に従って二酸化塩素 (CIO 2 )、水および 過塩素酸 (HCIO 4 ) に分解します。その塩から調製できます。 、塩素酸塩はより安定した化合物です。しかし、それは一般に 塩素 酸バリウムを介して得られ、 強酸 、通常は硫酸との反応により塩素酸が形成され、不溶性化合物である硫酸バリウムが 濾過 により反応媒体から除去される。塩の中でも塩素酸カリウムは重要で、花火や安全マッチの製造に頻繁に使用されます。実験室では、純粋な酸素ガスを得るために使用できます。製薬業界では、のど飴の製造に応用されています。
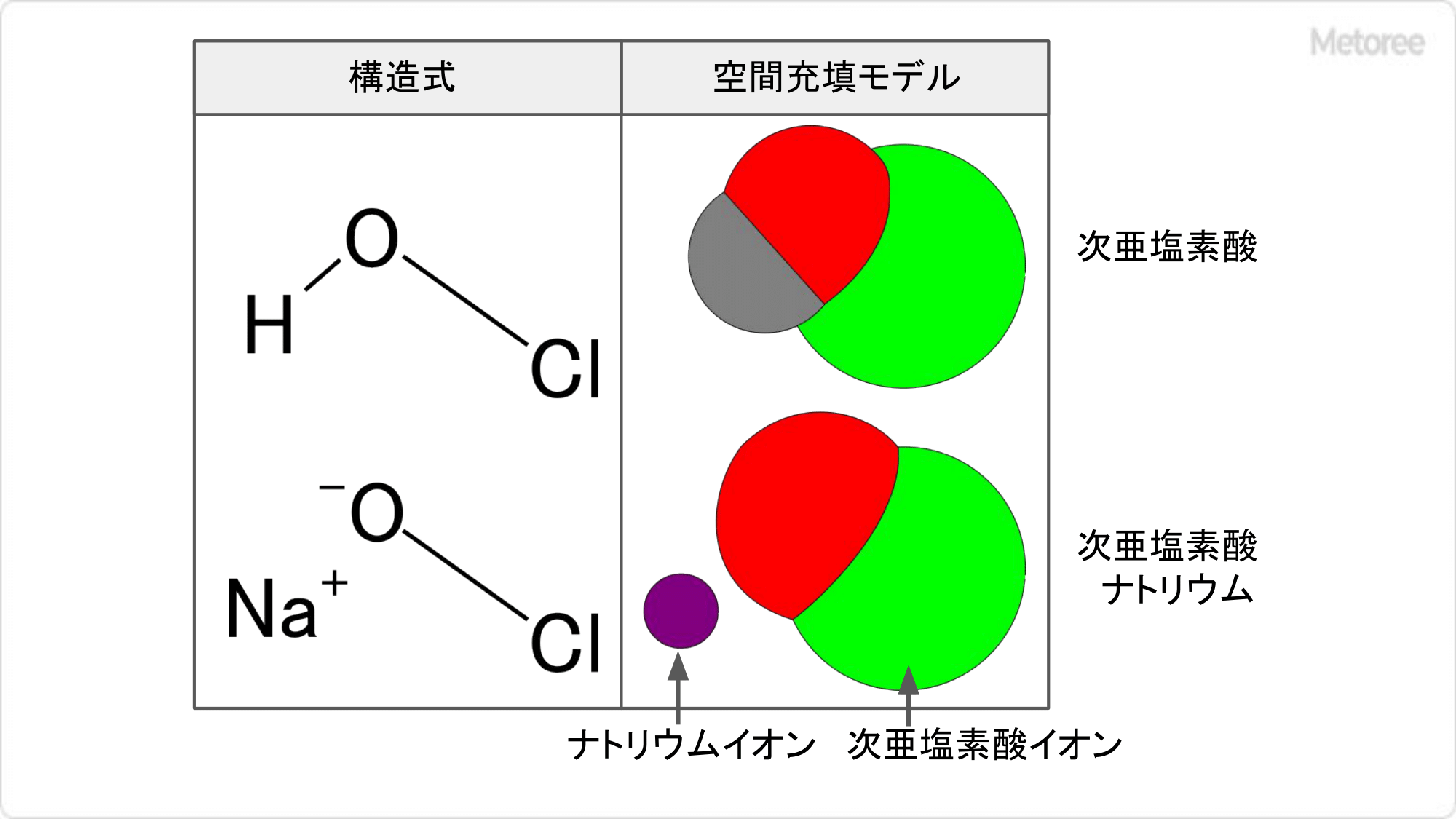
- 塩酸 : 研究室や産業界で非常に一般的で、水素化塩素または塩酸ガスの水溶液です。分子式はHClです。その応用性により、 ハロゲン 酸の中で最も重要なものとして注目されています。強い臭気があり、揮発性が高く窒息する可能性があるため、取り扱いには細心の注意が必要です。しかし、この酸の一般的な水溶液は塩酸ガスの濃度が 37 質量%であり、これがその溶液の最大濃度であり、濃塩酸として知られています。溶液中でも、既知の最も強い酸の 1 つであり、高い イオン化度 を持っています。その用途は、金属表面の洗浄から合成試薬としての使用まで多岐にわたります。
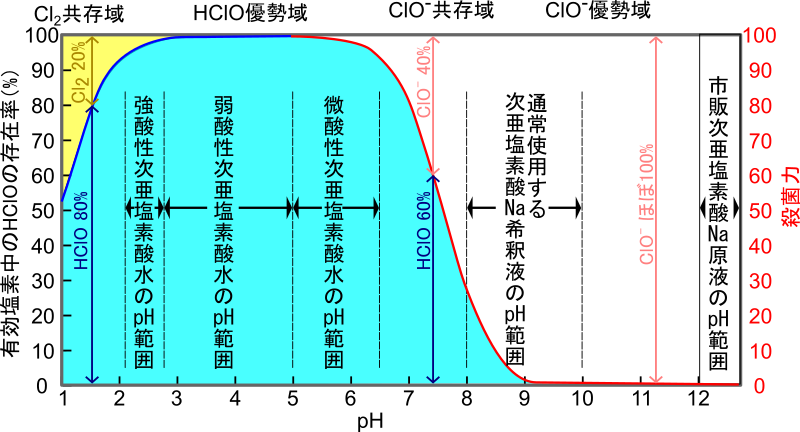
- 亜塩素酸 : 分子式 HClO 2 を持つ酸素含有酸 (オキシ酸)。これも塩素元素に由来します。自由形式では適用できません。
参考文献:
ネブレガ、ダ・シルバ。化学、単巻、初版、編。サンパウロ、アティカ/SP-2011。
ギャラリー