特定の植物を栽培するためには、水族館や土壌の水の pH と同じように、プールの水の pH も制御する必要がある、という声をよく聞きます。私たちの血液でさえ、pH を常に 7.35 ~ 7.45 に維持する必要があります。 0.4 の変動は致命的となる可能性があります。 pH とは正確には何ですか、またその値は何を意味しますか?

水のイオン積
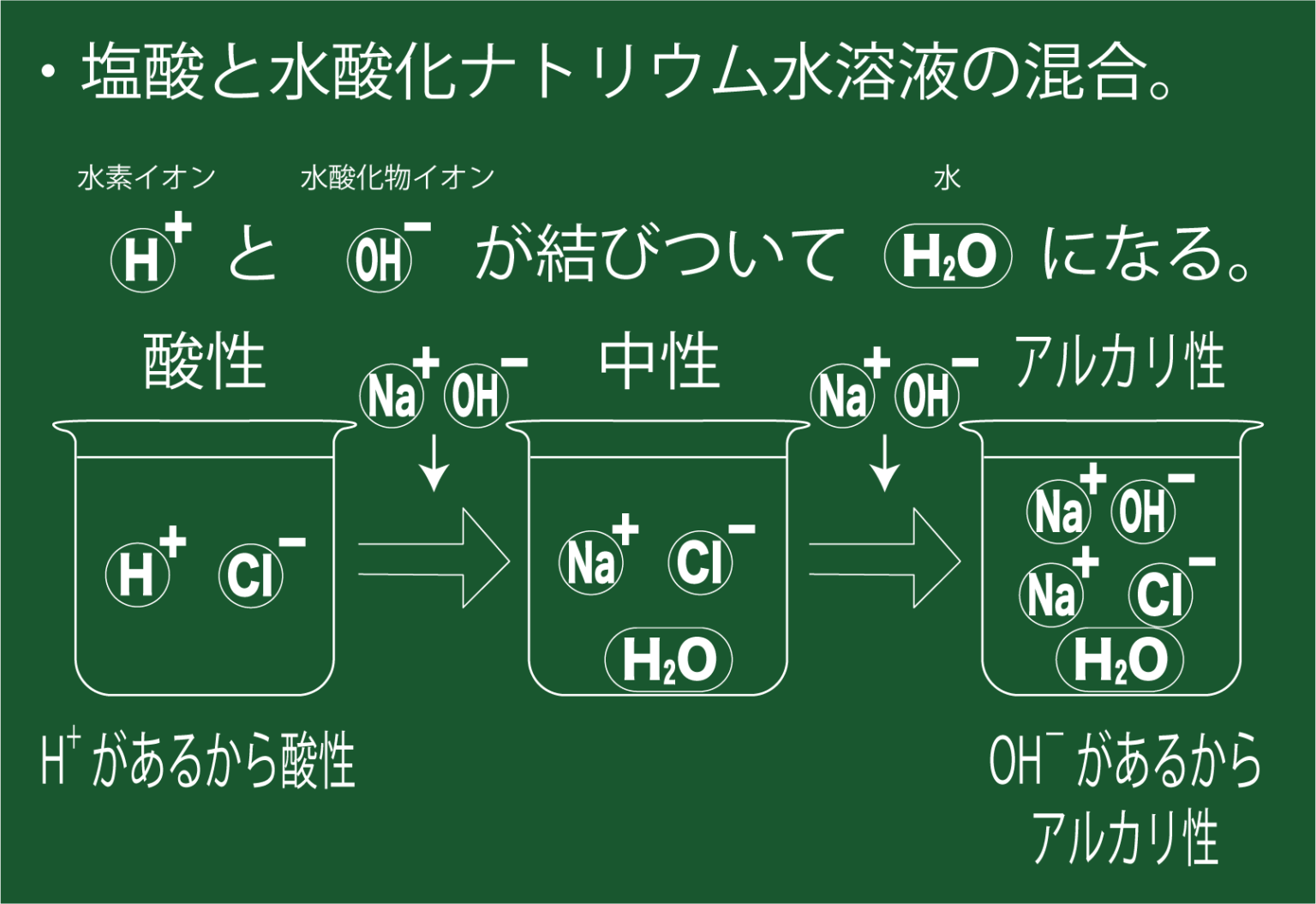
コップ一杯の水について考えてみましょう。この水はH2O分子だけで構成されているのでしょうか?いいえ、これらの分子は常に運動しているため、常にぶつかります。結果: 水分子は別の水分子と衝突して反応する可能性があります。生成されるバランスは、
水の
自己
イオン化
として知られています。
HOH ↔ H
+
+ OH
–
または
HOH + HOH ↔ H
3
O
+
+ OH
–
すでに知られているように、水の濃度 ─ [H
2
O] ≈ 55.6 mol/L ─ は、新しい物質 (たとえば、
酸
など) を加えて現在のような希薄な溶液を形成した場合、ほとんど変化しません。研究中です (これらの溶液の形成では、0.5 モルを超える水はほとんど消費されません。55.6 モルから開始して 55.1 モルの水で実験を終了することは、大きな変化ではありません)。したがって、[H
2
O] が定数であると考えます。
純水は中性であるため (H + イオン ごとに OH – イオンも形成されるため)、25 °C で [H + ].[OH – ] の場合、 [H + ] = [OH – ] となります。 = 1.0.10 -14 、[H + ] = [OH – ] = 10 -7 mol/L となります。
水の
モル濃度
は実質的に一定であり、平衡定数に戻るので、次のように書くことができます。
K.[H
2
O] = [H
+
].[OH
–
]
これにより、次のような 1 つの定数 (2 つの定数の積) が得られます。
K w = [H + ].[OH – ]
これはいわゆる水のイオン積で、ow は英語の水に由来します。
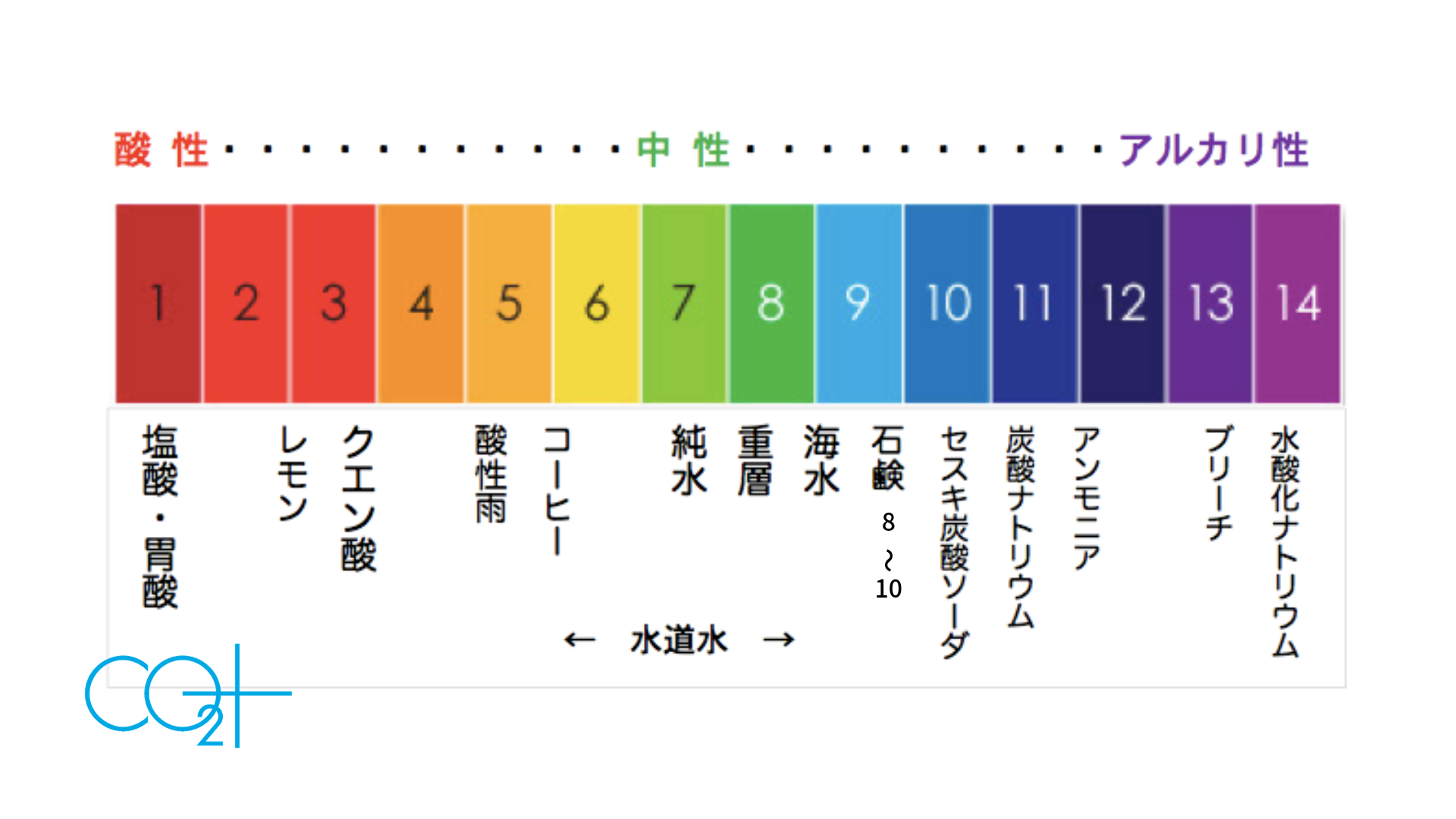
水溶液の性質
酸性溶液:
[H + ] > 10 -7 mol/L および [OH – ] < 10 -7 mol/L
基本的な解決策:
[H
+
] < 10
-7
mol/L および [OH
–
] > 10
-7
mol/L
中性溶液:
[H
+
] = 10
-7
mol/L および [OH
–
] = 10
-7
mol/L
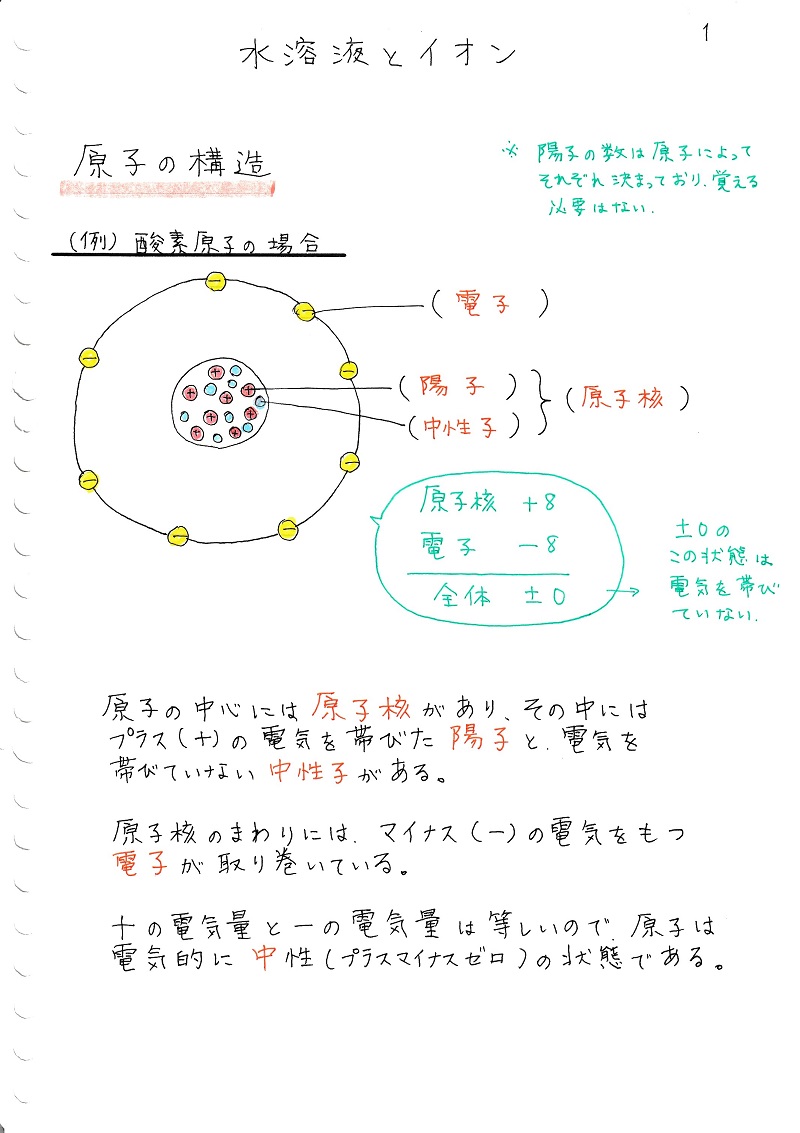
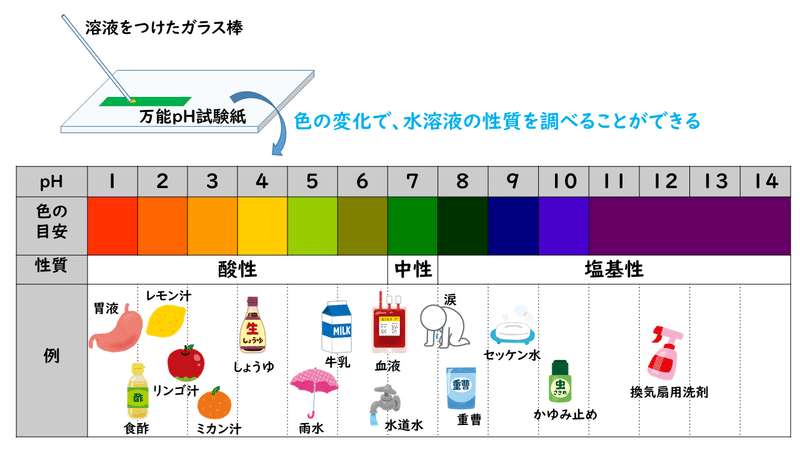
pH
セーレンセンは、pH を水素濃度の逆数の 対数 (10 進数) として定義しました。
pH = log 1/[H + ]
あるいは、水素濃度の 対数 としても次のようになります。
pH = コログ [H
+
]
つまり:
pH = log 1/[H
+
] → pH = log 1 – log [H
+
]
ログ 1 = 0 なので、次のようになります。
pH = -log[H
+
] または pH = colog [H
+
]
これは対数の逆数に等しい。
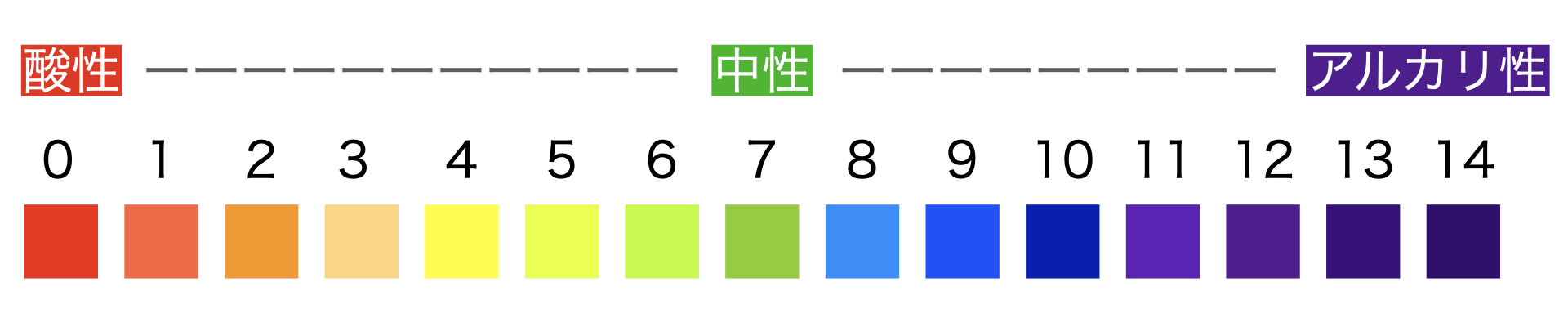
25 °C での H + と OH – の濃度に応じた pH の変化を見てみましょう。
中性媒体: pH = 7
酸性媒体: pH < 7
基本培地: pH > 7

pOH
同様に、pOH はヒドロキシル濃度の逆数の対数 (10 進数) として定義されます。
pOH = log 1/[OH – ]
または、OH – 濃度の対数として:
pOH = コログ [OH
–
]
このような:
pOH = log 1/[OH – ] → pOH = log 1 – log [OH – ]

ログ 1 = 0 なので、次のようになります。
pOH = -log[OH – ] または pOH = colog [OH – ]
OH – と H + の濃度に応じた pOH の変化を見てみましょう。
中性媒体: pOH = 7
酸性媒体: pOH > 7
基本培地: pOH < 7
pHとpOHの関係:
pH + pOH = 14 (25 °C)

観察:
pH と pOH の概念は、あらゆる溶液中に H + と OH – が共存することを示します。溶液がどれほど酸性であっても、少数ではありますが、常に OH – イオンが存在します。塩基性溶液には、H + イオンも存在します。これらのイオンの濃度が互いに打ち消し合うことはありません。
ギャラリー