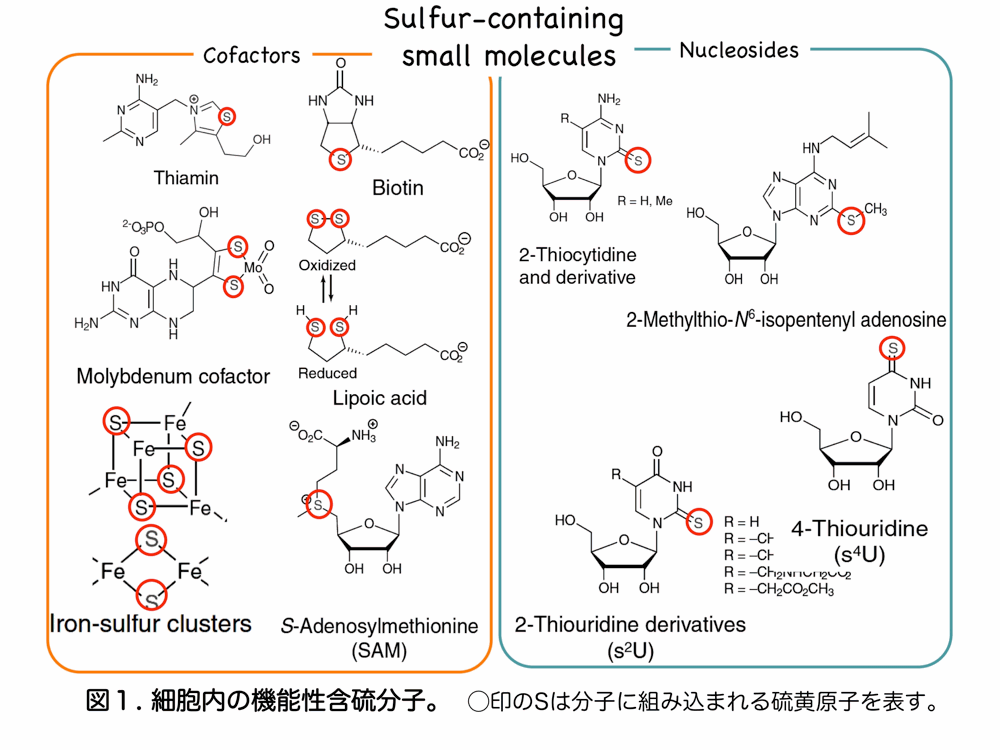
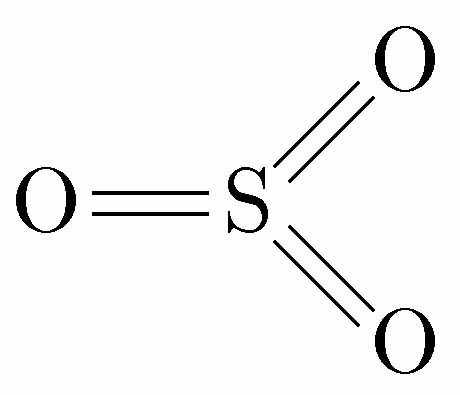
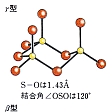
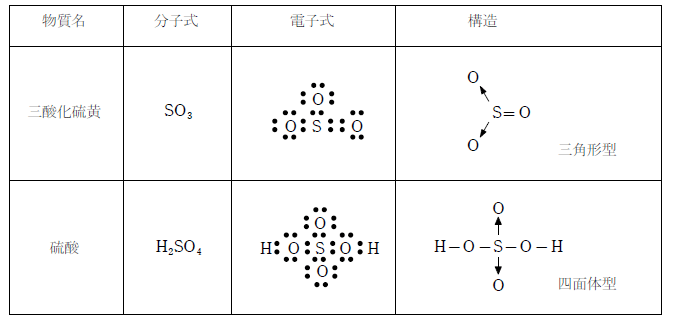
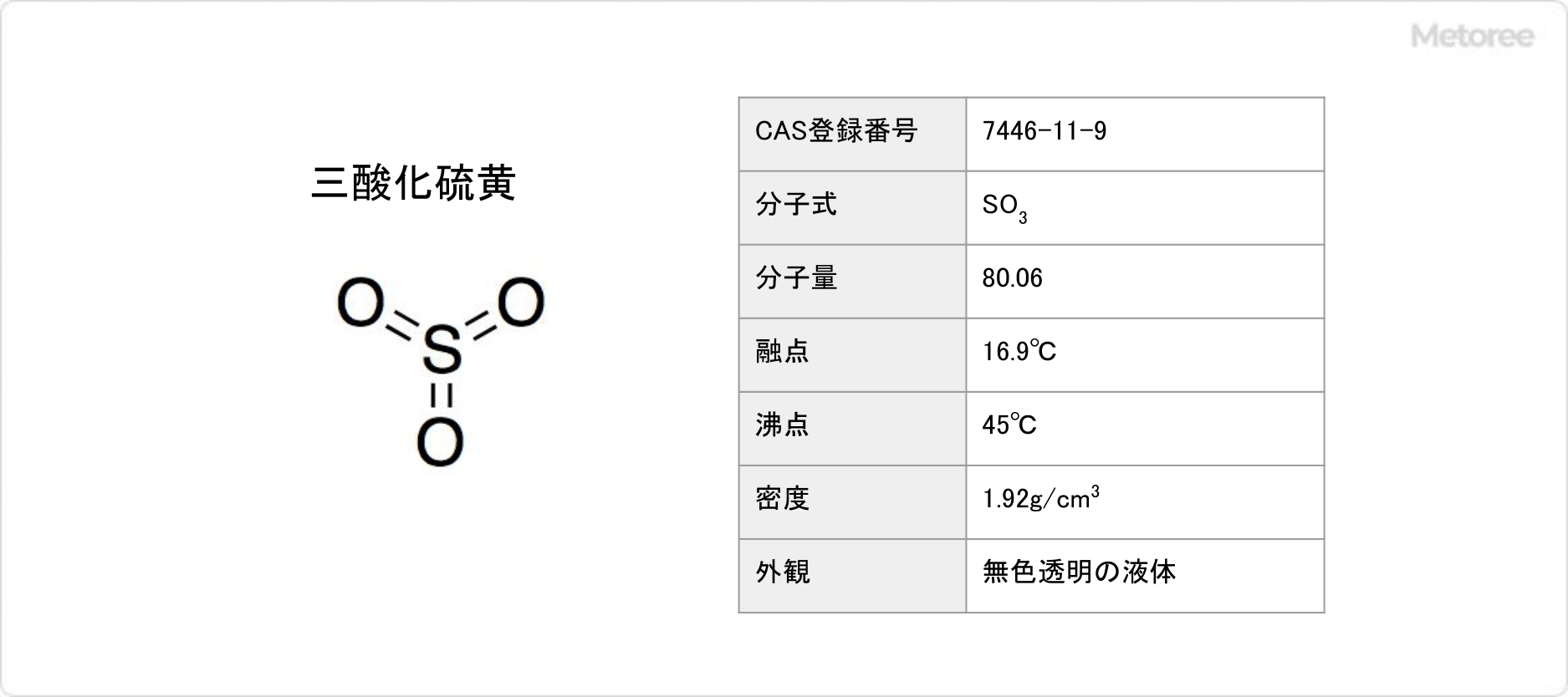
三酸化硫黄は 、S 原子と O 原子の間の共有二重結合によって形成される 分子 で、その分子式は SO 3 です。 S=O 結合間の角度が 120 度の平らな三角形状をしているため、分子の双極子モーメントはゼロとなり、非極性の性質を持ちます。 無水硫酸 または 酸化硫黄 としても知られ、硫黄原子の酸化状態は +6、形式電荷は +3 です。 SO 3 分子の分子量は 80.06 g/mol、 融点と沸点は それぞれ 16.9 ℃と 45 ℃です。室温では、密度 1.92 kg/m 3 の無色の煙の出る液体の形で見られます。ガス状の場合、それは汚染性、刺激性、腐食性の化合物であり、 酸性雨 の主な原因の 1 つです。 SO 3 によって引き起こされる健康上の問題には、 呼吸器疾患 、特に気管支炎、さらに深刻な場合には 肺気腫 や心血管疾患があります。これは安定した化合物ですが、有機物、 金属 、塩基、シアン化物とは相溶せず、水や 酸素 と強く反応します。これは非常に吸湿性があり、その水和熱により木材や綿が発火する可能性があります。これは、これらの材料の構造に存在する 炭水化物 が脱水されるためです。
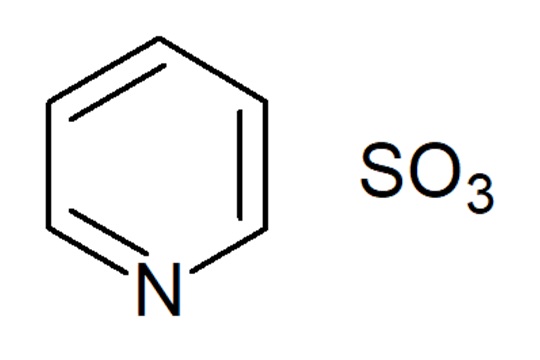
SO 3 は 、反応触媒として 五酸化 バナジウム(V 2 O 5 )の存在下、精製 二酸化硫黄 (SO 2 )と大気中の酸素との反応(温度400~600℃)によって得られます。このプロセスは直接接触と呼ばれ、触媒は珪藻土またはシリカに担持された酸化カリウムによって活性化されます。
この反応は可逆的であり、制御された温度でゆっくりと起こりますが、温度が上昇すると平衡状態が SO 2 と O 2 の生成に向かう可能性があります。 SO 3 を失わずに反応を速くするために、硝酸カリウムベースの 触媒 を追加できます。
SO 2 + NO 2 → SO 3 + NO
315℃での脱水: 2 NaHSO 4 → Na 2 S 2 O 7 + H 2 O
460℃での亀裂: Na 2 S 2 O 7 → Na 2 SO 4 + SO 3

SO 3(g) + H 2 O (l) → H 2 SO 4(l)
この反応は、 強酸 である H 2 SO 4 の存在が雨水の pH を低下させるため、SO 3 が 酸性雨の問題に寄与するガスの 1 つである理由を説明します。これは、水生環境や土壌のpHを変化させ、これらの生態系に不均衡を引き起こすため、一連の問題を引き起こします。さらに、酸性雨は都市に被害をもたらし、 腐食 プロセスによって記念碑、建物、橋、車両、さらには 塗装さえ も破壊します。
SO 3 によって引き起こされる健康と環境の問題のため、 SO 3 は国家環境評議会 (CONAMA) の大気質指標のリストに含まれています。
参考文献:
アトキンス、P.W.ジョーンズ、ロレッタ。化学の原理: 現代の生活と環境への疑問。単巻。第3版ポルトアレグレ:ブックマン、2006年。
カルドーソ、AA; Pitombo、LRM 環境硫黄貯蔵量の世界的なバランスに対する、削減された 硫黄 化合物の貢献。キミカ・ノヴァ、v. 15、p. 219、1992年。
大気質指標国家環境評議会 (CONAMA)、 http://www.mma.gov.br/port/conama/ で入手可能 (2019 年 4 月にアクセス)。
Kotz、JC 一般化学と化学反応。第 1 巻、第 9 版、Cengage Learning、2015 年。

ティトとカント。日常的なアプローチにおける化学。 1 冊、パート A およびパート C – 有機化学。編集者サライバ、2005 年。
ルイジアナ州シルバ。カルヴァーリョ、LS;ワシントン州ロペス。ペレイラ、ペンシルベニア州デパウロ。 Andrade、JB ガスの溶解度と反応性。 Química Nova、Vol. 40、No. 7、824-832、2017
ギャラリー