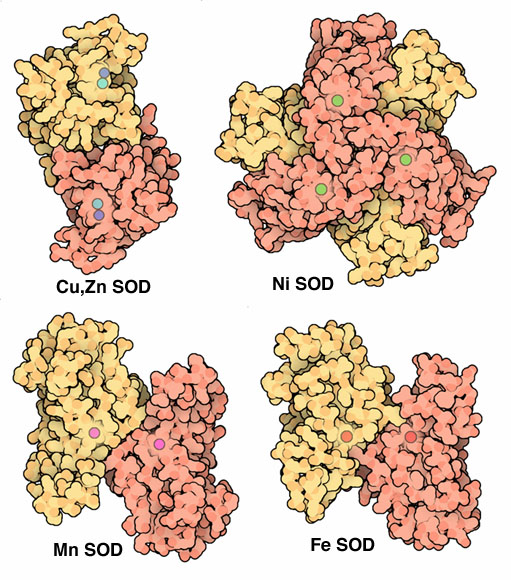
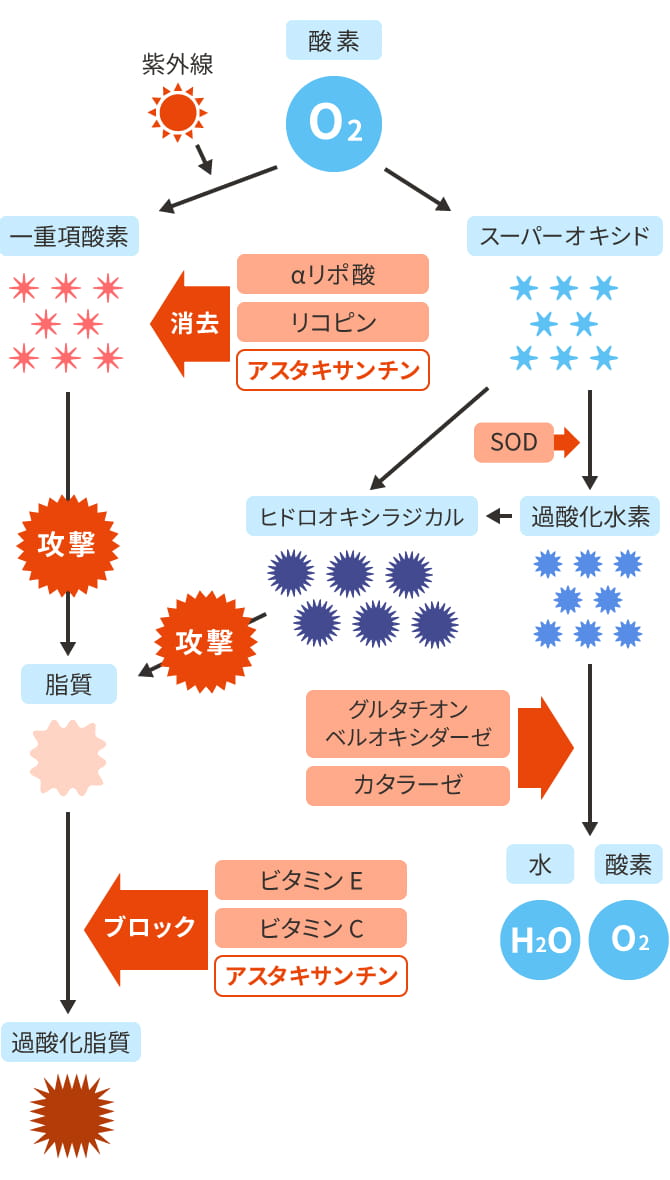
スーパーオキシドは 、その構造内に陰イオン O 2 – を持つイオン性化合物で、酸素の 酸化状態は 、ほとんどの 無機化合物 のように -2 ではなく、-1/2 になります。 O 2 アニオン – ラジカル種であり、O 2 分子 よりも 1 つ多い電子を持ち、この電子は対になっていないため、常磁性種です。これらは、分子状酸素の還元によって生成される、最も活性な酸素種の 1 つであると考えられています。

O 2 + および – → O 2 •-
これらは 二元化合物 、つまり 2 つの元素で形成され、一方は 酸素 、もう一方は アルカリ金属 (Li、Na、K、Rb、Cs、Fr) または アルカリ土類金属 (Be、Mg、Ca) です。 、ミスター、バ、ラ)。これらは水または酸と反応して過酸化水素 (H 2 O 2 ) を生成します。物理的状態に関しては、室温では固体の形で見られます。
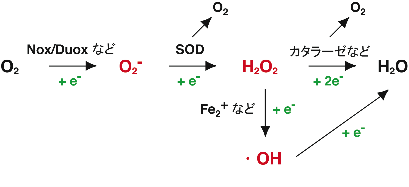
スーパーオキシドは 生物 の体内に存在します。そして、これはどうして起こるのでしょうか? 好気呼吸 の過程では、酸素分子 (O 2 ) が 電子 受容体として機能し、特定の状況下では電子を 1 つだけ受け取るため、スーパーオキシドが生成されます。スーパーオキシドは非常に有毒な化合物であり、 免疫系 によって外来微生物を破壊するために使用されます。特定の白血球は、 細菌 を破壊するために使用されるスーパーオキシドを生成する酵素 NADPH オキシダーゼを持っています。しかし、 白血球 や好気性 代謝 反応によって生成されるスーパーオキシドは フリーラジカル を生成する可能性があり、これらが害を及ぼさないように、私たちの代謝には酸素と過酸化水素への不均化を促進する酵素スーパーオキシドジスムターゼが存在します。この過酸化物は、後に酵素カタラーゼの作用によって元素状の H 2 O と O 2 に分解されます。
超酸化物の例としては、CsO 2 、RbO 2 、KO 2 および NaO 2 の塩があり、これらは O 2 とそれぞれの 金属 の反応によって形成されます。これらの塩は水に溶解すると、 過酸化水素 、酸素、塩基を形成します。この反応は次のように表すことができます。
2O2 ・- + 2H2O → O2 + H2O2 + 2OH−
この反応では、O 2 ・- は 強いブレンステッド塩基 として機能します。水が存在しない場合でも、加熱すると、スーパーオキシドは過酸化物と水に分解します。

2MO2 → M2O2 + O2
形成される過酸化物は、O 2 – に結合する金属 (M) によって異なります。
宇宙飛行士がどのようにして宇宙でこれほど長い時間を過ごし、客室内の 酸素が 不足することがないのか、立ち止まって考えたことはありますか?したがって、これを担当するのはスーパーオキシド KO 2 です。これは、次の反応のように、潜水艦、宇宙船、地下鉱山などの閉鎖環境で空気を再生するために使用される化学酸素発生装置で使用されます。

CO 2(g) + 4 KO 2(s) → K 2 CO 3(s) + 3O 2(g)
さらに、この化合物は呼吸器から CO 2 と水を除去するために使用できます。
スーパーオキシドの命名法に関しては、金属は固定酸化数 (NOX) を持つアルカリおよびアルカリ土類族に属するため、次の順序に従ってください。

スーパーオキシド+金属名
例: LiO 2 – 超酸化リチウム。 MgO 4 – 超酸化マグネシウム。
参考文献:
アトキンス、P.W.ジョーンズ、ロレッタ。化学の原理: 現代の生活と環境への疑問。単巻。第3版ポルトアレグレ:ブックマン、2006年。
Kotz、JC 一般化学と化学反応。第 1 巻、第 9 版、Cengage Learning、2015 年。
ティトとカント。日常的なアプローチにおける化学。 1 冊、パート A – 一般および無機化学。編集者サライバ、2005 年。
ギャラリー