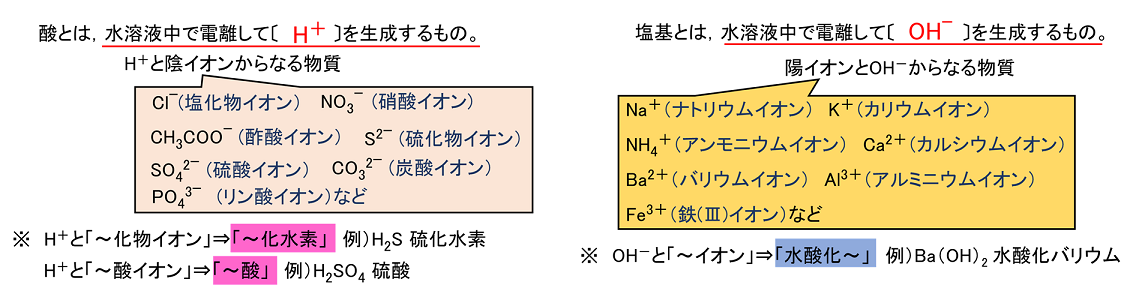
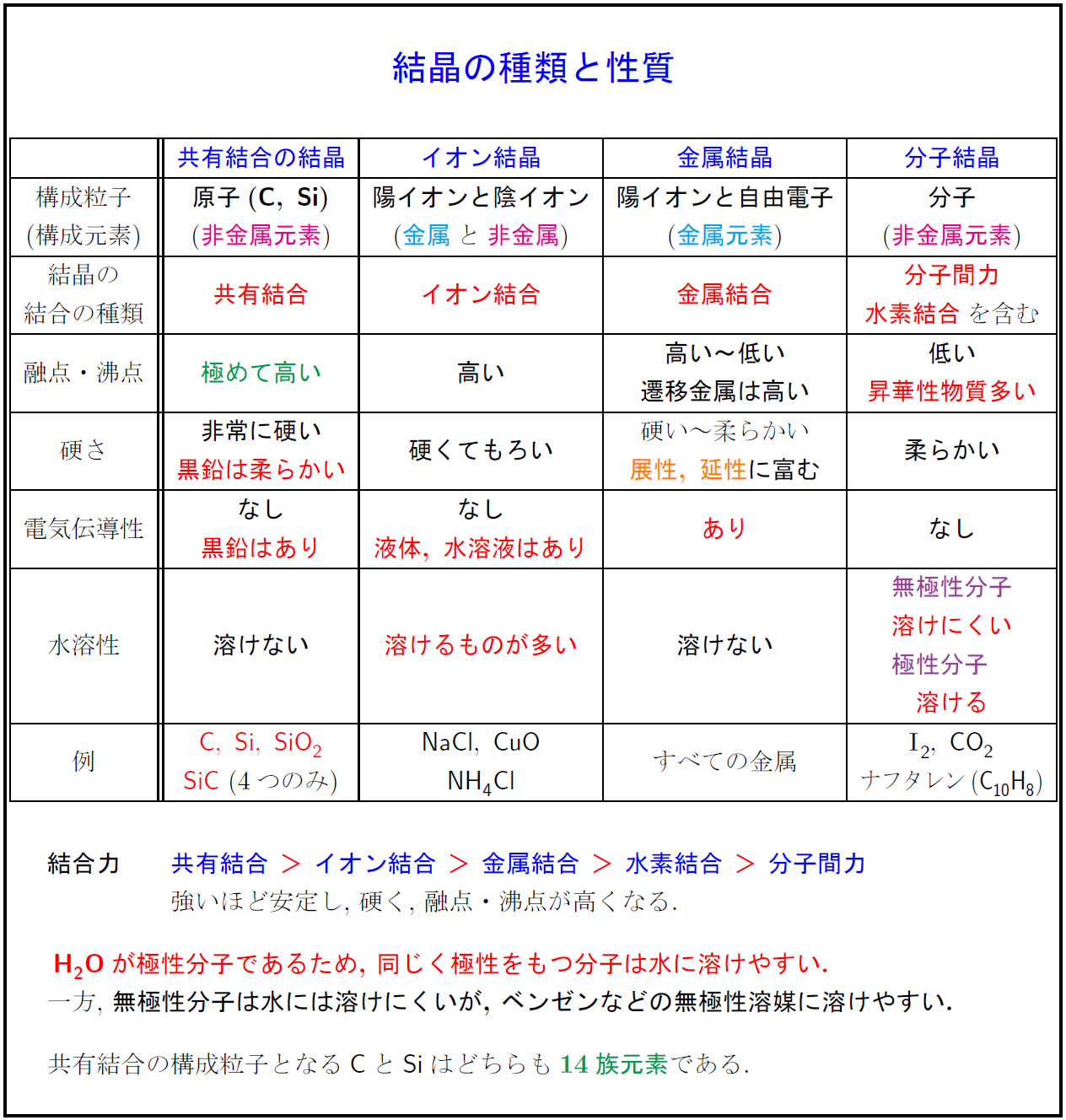
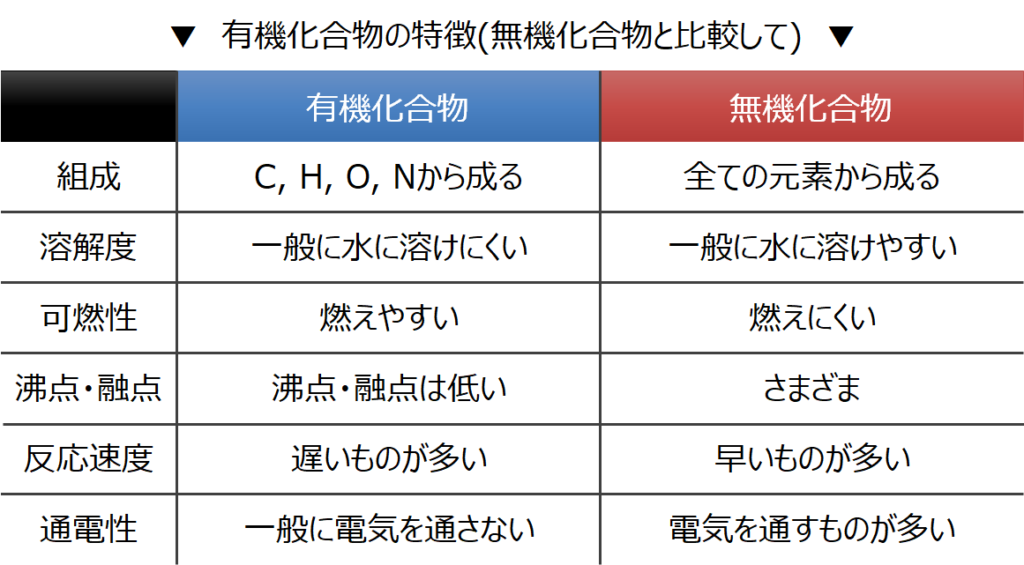
化学機能は、同様の特性を持つ化合物のグループによって特徴付けられます。最初は、無機化合物 (一部の例外を除き、 炭素 を含まない化合物) と有機化合物 (炭素を含む化合物) が存在します。 無機化学 で研究される機能は、 酸 、 塩基 、塩、 酸化物 の 4 つです。
無機機能を同定するための理論的手段として、化合物の分子式に基づいて、以下の表に確立された基準を採用できます。
|
関数 |
から始める |
までに終了 |
観察 |
|---|---|---|---|
|
酸 |
H + カチオン |
||
|
基礎 |
アニオンOH – |
||
|
塩 |
H + 以外のカチオン |
OH以外の陰イオン – |
|
|
酸化物 |
アニオン O2- |
バイナリ |
酸は、その物理的および化学的挙動に応じて、以下の基準に従っていくつかの重要な分類が認められます。
この記事の内容
水素の数について
- 一酸または単プロトン酸: 分子内にイオン化可能な水素が 1 つだけあります。例: 塩酸 (HCl)。
- 二酸または二プロトン酸: 分子内に 2 つのイオン化可能な水素があります。例: 硫酸 (H 2 SO 4 )。
- 三酸または三プロ酸: 分子内に 3 つのイオン化可能な水素があります。例: リン酸 (H 3 PO 4 )。
素子数について
- バイナリ: 分子内に 2 つの異なる要素のみが存在します。例:臭化水素酸(HBr)。
- 三元系: 分子内に 3 つの異なる要素があります。例:リン酸(H 3 PO 4 )。
- 四次: 分子内に 4 つの異なる要素があります。例: チオシアン酸 (HSCN)。
酸素の存在について

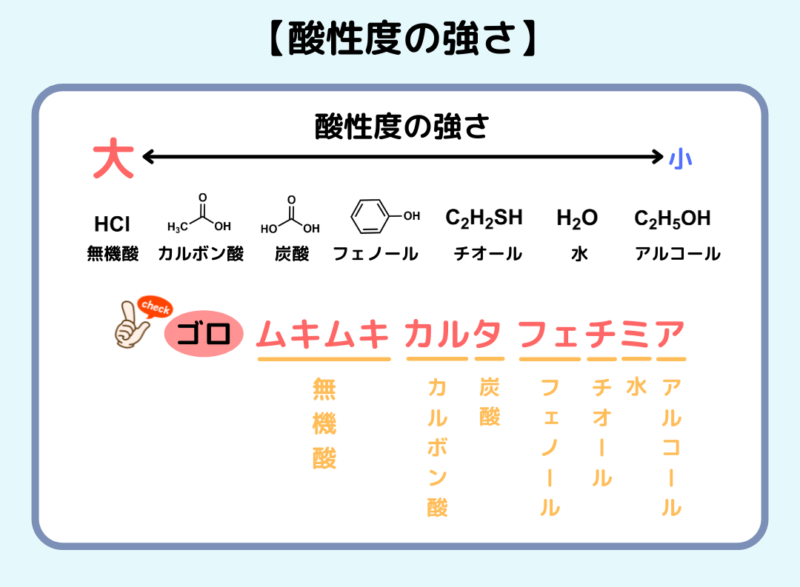
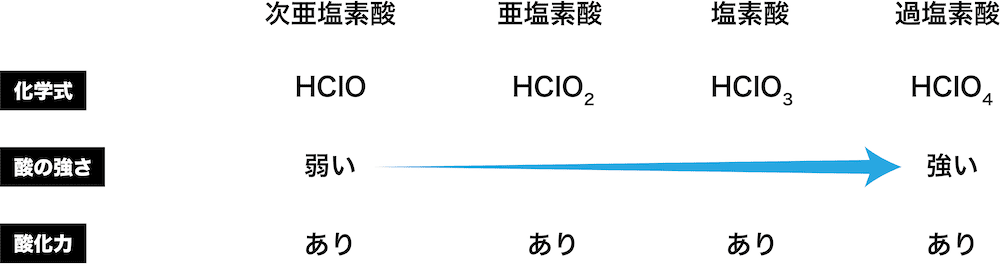
イオン化度(酸性の強さ)について
- 強水素酸とは、 ハロゲン である 塩素 、 臭素 、または ヨウ素 を含むものです。例:塩酸(HCl)。
- オキシ酸に関しては、分子内の 酸素 原子の数が 水素 原子の数だけ減ります。答えが 2 以上の場合、酸が 強い と考えられます。例:硫酸(H 2 SO 4 )。
- すべての 有機酸 ( 炭酸 、H 2 CO 3 、有機ではないが弱い 青酸 HCN を除く炭素を含む)を含む、上記のルールのいずれにも当てはまらない酸はすべて酸とみなされます。イオン化度が低いため、 弱いです 。
提示された酸の分類によれば、塩酸と硫酸はそれぞれ以下のように分類できます。
- HCl: 一酸、二成分、水酸、強酸。
- H 2 SO 4 : 二酸、三元酸、酸素酸、強酸。
参考文献:
アトキンス、ピーター。ロレタ・ジョーンズ。化学の原理: 現代生活と環境への疑問、ポルト アレグレ: ブックマン、2001 年。
フェルトレ、リカルド。化学の基礎、vol.ウーニコ、モデルナ編、サンパウロ/SP – 1990 年。
ペルッツォ、フランシスコ・ミラガイア(チトー)。カント、エドゥアルド・レイテ。 Chemistry in the Everyday Approach、現代編、vol.1、サンパウロ/SP- 1998。
ギャラリー