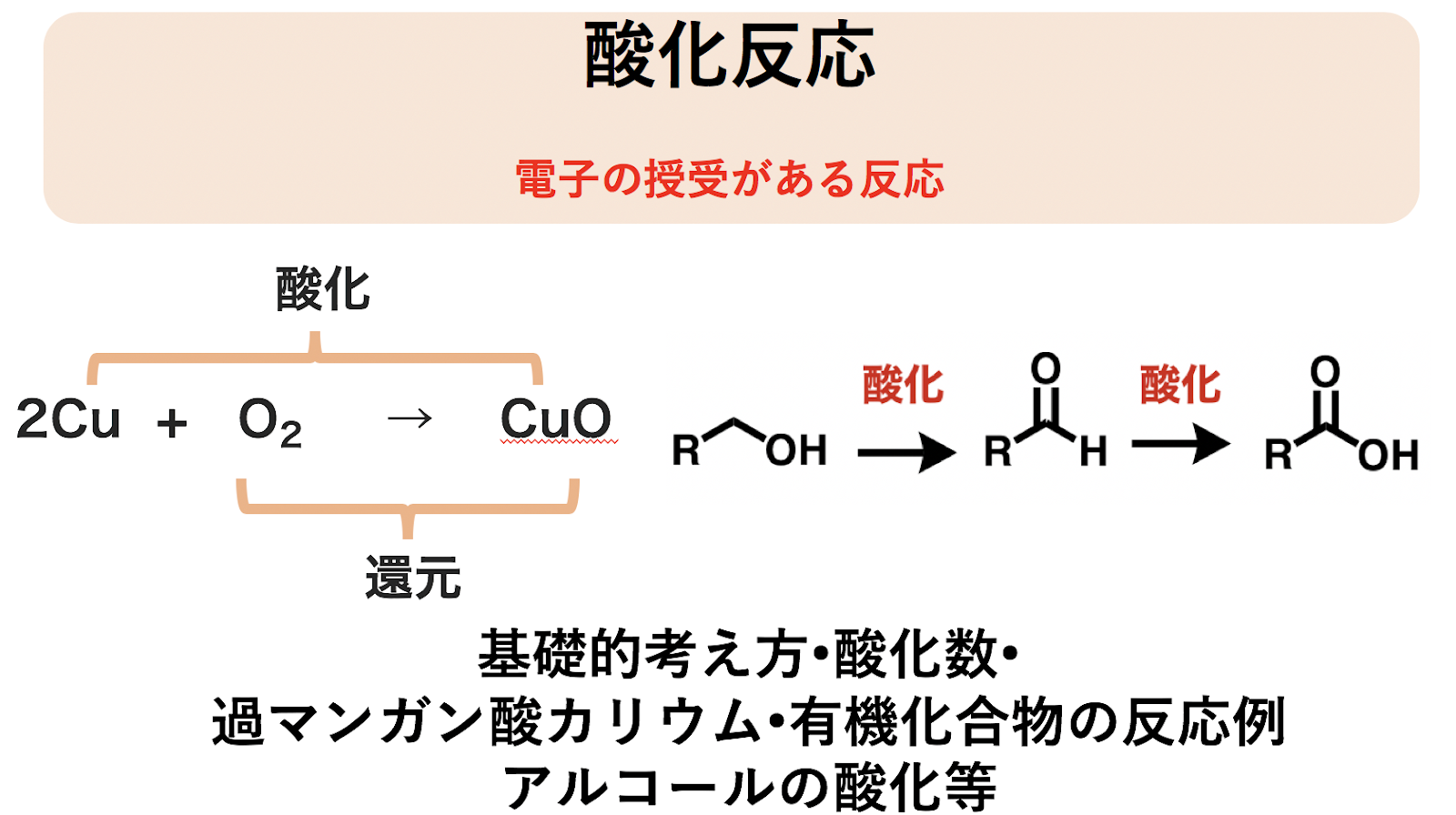
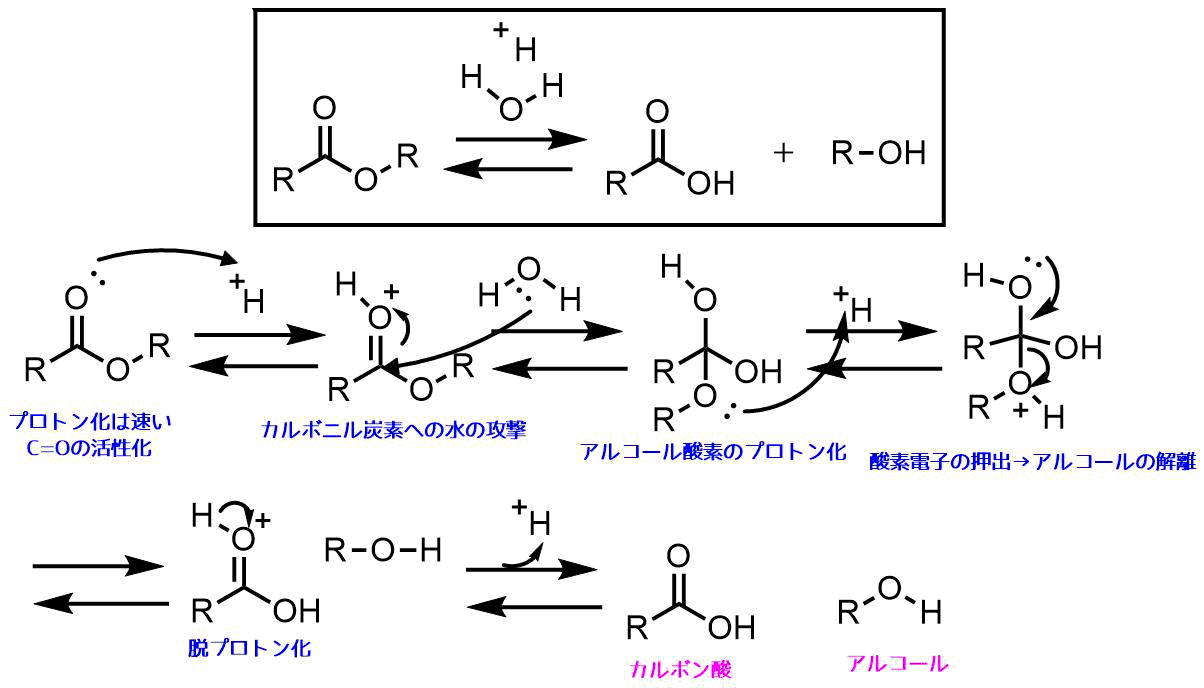
二重交換反応
または
メタセシス
反応は、文字通り、反応に関与する各分子の要素間で交換が行われることを特徴とします。言い換えれば、特定の原子、
イオン
、またはラジカルが位置を変え、別の分子に移動し、その位置にあった原子、イオン、またはラジカルと置き換わります。以下はメタセシス反応を例示する一般的な反応です。
二重交換反応
または
メタセシス
反応は、文字通り、反応に関与する各分子の要素間で交換が行われることを特徴とします。言い換えれば、特定の原子、
イオン
、またはラジカルが位置を変え、別の分子に移動し、その位置にあった原子、イオン、またはラジカルと置き換わります。以下はメタセシス反応を例示する一般的な反応です。

AB + CD -> AC + BD
ここで、AB と CD は同時に固体になることはできませんが、液体と固体の組み合わせ (液体 + 液体、液体 + 固体、または固体 + 液体) になります。そして同時に、二重交換反応の特徴として、生成物は以下の側面の少なくとも 1 つにおいて反応物と異なっていなければなりません。
1) AC および/または BD は、AB および/または CD よりも溶解性が低くなければなりません。
H 2 SO 4(aq) + Ba(OH) 2(aq) -> 2H 2 O (l) + BaSO 4(s)
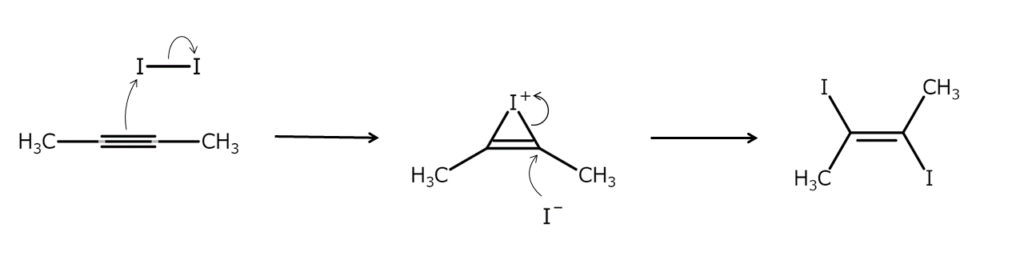
2) AC および/または BD は、AB および/または CD よりも弱い電解質でなければなりません。
この要件は、反応生成物の 1 つがイオン化性が低くなければならない、つまり、反応物に対して 電気伝導性 が低くなければならないことを意味します。塩酸と 水酸化ナトリウム (苛性ソーダ) の間の 中和反応 では、NaCl (溶液中または溶融状態にかかわらず優れた伝導体) と液体の水が形成されます。液体の水は伝導体ではなく、他のものとは異なります。
HCl (水溶液) + NaOH (水溶液) -> NaCl (水溶液 ) + H 2 O (l)
3) AC および/または BD は、AB および/または CD よりも揮発性が高くなければなりません。

NaHCO 3(s) + HCl (aq) -> NaCl (s) + H 2 CO 3(aq) -> NaCl (s) + H 2 O (l) + CO 2(g)
二重交換反応のもう 1 つの大きな特徴は、反応物は交換ではなく合成で反応する傾向があるため、一般に 酸化物 ではないことです。したがって、二重交換反応とは、酸と 塩基 (中和)、2 つの塩 (不溶性のものと)、塩と酸 (別の塩と別の酸を形成)、または塩と塩が反応する反応です。塩基(別の塩と別の塩基を形成する)。
すべての二重交換反応インジケーターの中で、沈殿物の形成を識別するのが最も簡単です。より揮発性の高い生成物やイオン化されにくい生成物の検出は、補完的な実験を通じてのみ可能です。したがって、この効果を生み出す反応は、高校の化学学生の訓練期間中の学校の研究室で好まれます。
https://web.archive.org/web/20121102191721/http://www.scribd.com/doc/3395764/Quimica-Aula-08-Reacoes-de-dupla-troca (2010 年 2 月 28 日にアクセス)
https://web.archive.org/web/20130723060129/http://www.scribd.com/doc/4489649/AULA-53-REACOES-DE-DUPLATROCA (2010 年 2 月 28 日にアクセス)
http://pt.wikipedia.org/wiki/Reação_de_dupla_troca (2010 年 2 月 28 日にアクセス)
ギャラリー