化学元素の周期的特性は、 周期表 内の位置、つまり原子番号に従って変化する、これらの元素に固有の特性です。
周期的特性は、 電気陰性度 、電気 陽性 度、 原子半径 、 電子親和力 、 イオン化 ポテンシャル 、 原子密度 、 原子体積 、 融解 温度 、 沸点 です 。最後の 4 つの特性は、ある種の乱れを示すため、非 周期的 であると考えられます。つまり、原子の体積は、周期内で中心から端に向かって増加します。融解温度と沸騰温度は、左側の族 (1A および 2A) では原子半径とともに増加し、右側の族 ( 希ガス と ハロゲン ) では減少します。
最も研究されているプロパティは次のとおりです。
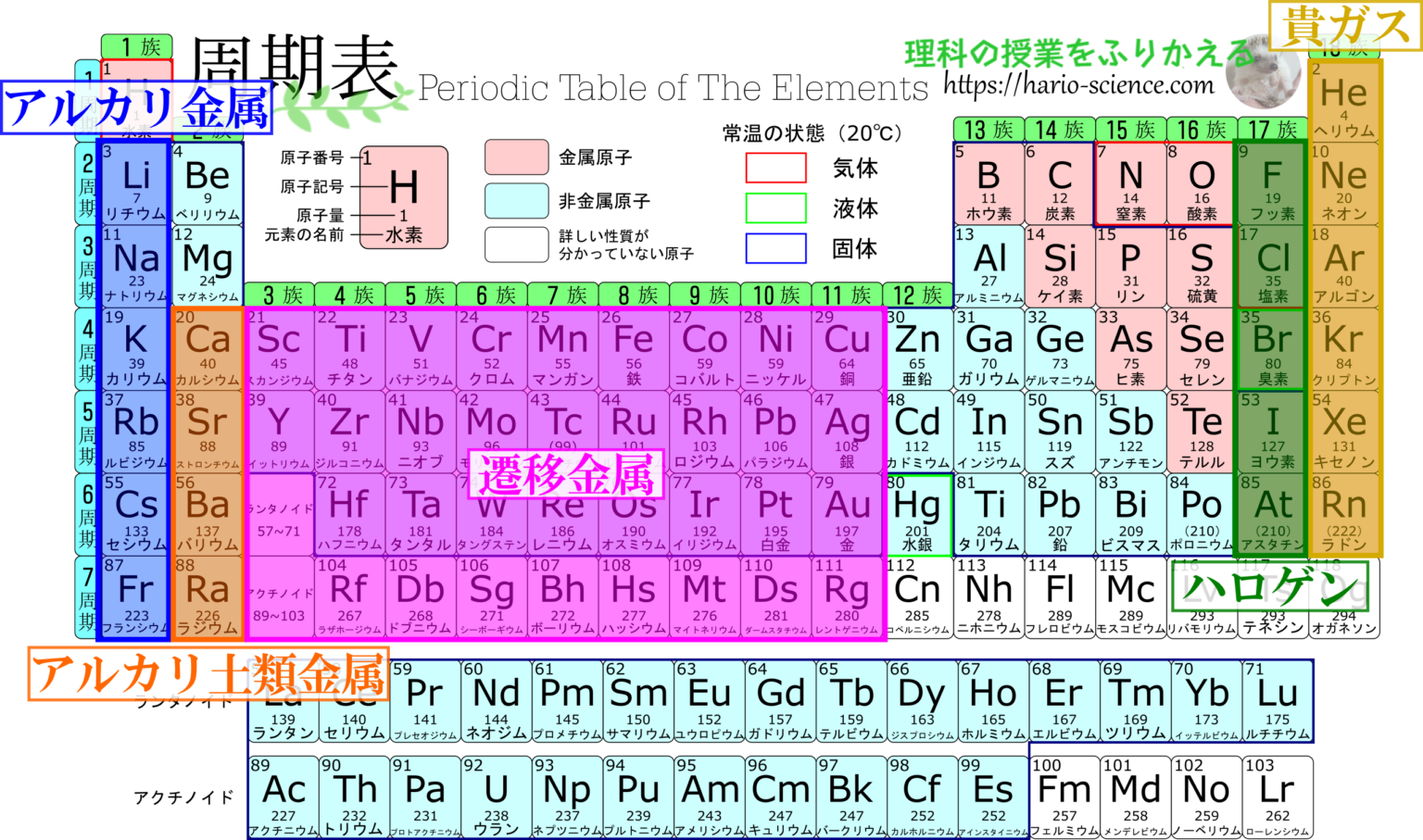
電気陰性度
最もよく使用される ポーリング スケールは 、原子半径の減少と原子核と 電子圏 の間の相互作用の増加により、電気陰性度が下から上に向かって族内で増加すると定義します。原子番号の増加に伴う左から右の期間。
フッ素は 周期表上で最も電気陰性の元素です。

 電気陽性
電気陽性
電気陽性度の測定方法は電気陰性度と同じで、化学結合によって測定されます。ただし、原子が電子を失う傾向を測定するため、意味は逆であり、 金属が 最も電気陽性です。
電気陽性は電気陰性とは反対の方向に成長します。家族では上から下に、期間では右から左に成長します。
フランシウム は最も電気的に陽性な元素であるため、酸化する傾向が最も大きくなります。
 注: 希ガスは非常に不活性であるため、電気陰性度および電気陽性度の値は、これらのデータを取得することが難しいため、研究の対象ではありません。
注: 希ガスは非常に不活性であるため、電気陰性度および電気陽性度の値は、これらのデータを取得することが難しいため、研究の対象ではありません。
原子半径
原子半径は基本的に、原子核から最外層の電子圏までの距離です。ただし、原子は剛体ではないため、固体化学結合における同じ元素の 2 つの原子の核中心間の距離の半分として定義される平均原子半径は、次のように計算されます。
原子半径は、各元素の原子の層数に従って、族内で上から下に増加します。ピリオドでは右から左へ。
その周期内の元素の原子番号が大きいほど、原子核と電子圏の間に働く力が大きくなり、その結果、原子半径が小さくなります。
既知の原子半径が最も大きい元素は セシウム ですが、フランシウムの原子半径がより大きい可能性が非常に高いですが、この元素は自然界では希少であるため、これはまだ確認されていません。
電子的親和性
電子親和力は、基底状態および気体状態の原子が電子を受け取ったときに放出するエネルギーを測定します。または、特定の元素の陰イオンから電子を除去するために必要な最小エネルギーさえも。
希ガスでは、やはり電子親和力は重要ではありません。ただし、電子が元素に追加されるとエネルギーが放出されるため、これはゼロにはなりません。
電子親和力は、周期表での成長において明確な形状を持ちませんが、その動作は電気陰性度に似ており、下から上、左から右に成長します。
塩素の 電子親和力はより高く、約 350 KJ/mol (弾性率) です。
イオン化電位
イオン化ポテンシャルは、 電子親和力の逆を測定します。つまり、基底状態および気体状態の中性原子から電子を除去するのに必要なエネルギーです。したがって、最初の電子の引き出しに必要なエネルギー量は 2 回目の電子引き出しより少なく、さらに 3 回目の電子引き出しよりも少なくなります。
電子親和力や電気陰性度と同じ挙動を示します。したがって、フッ素と塩素は周期表で最も高い電子親和力値を持つ元素であるため、周期表で最も高いイオン化ポテンシャルを持つ原子であると言えます。
ギャラリー


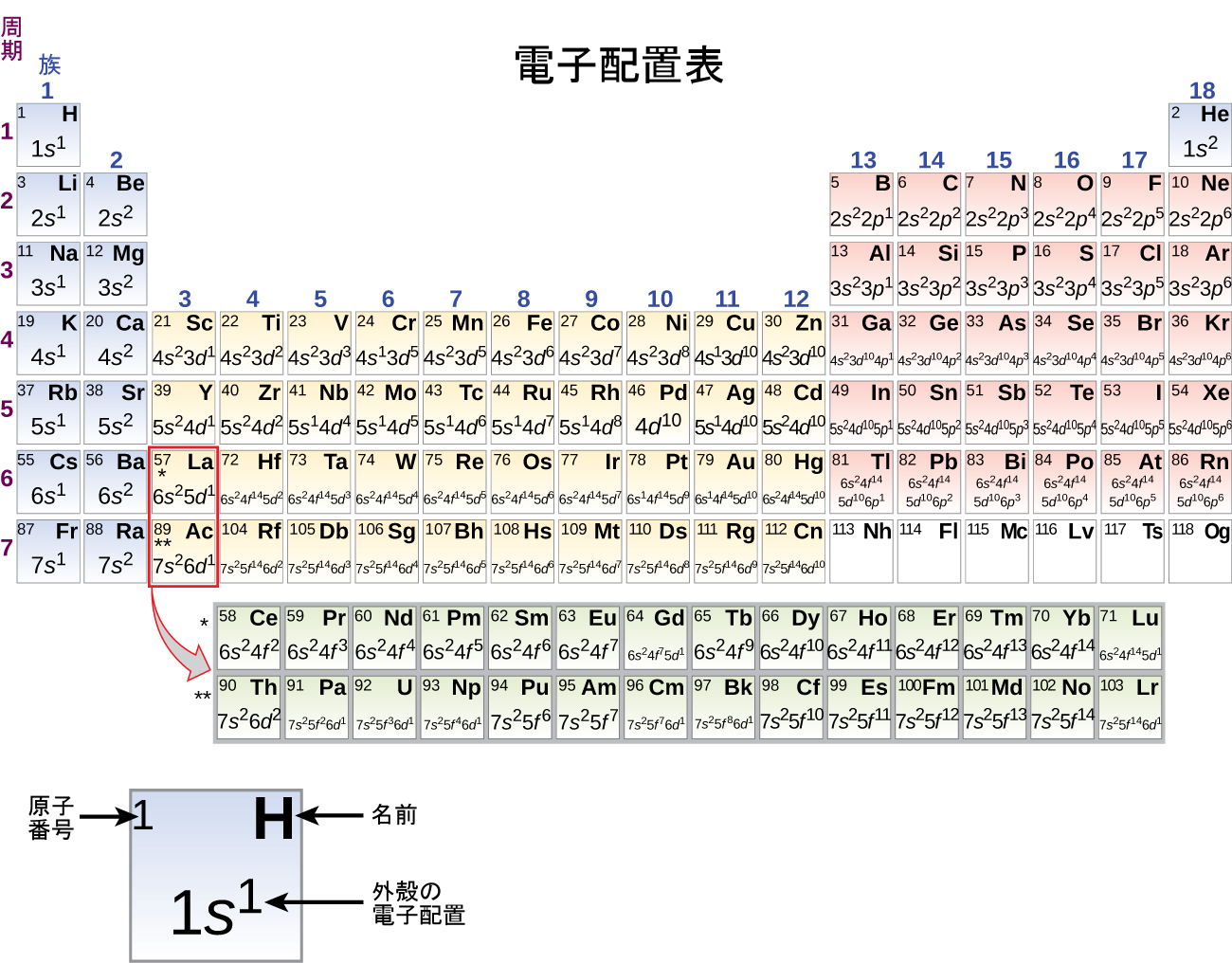





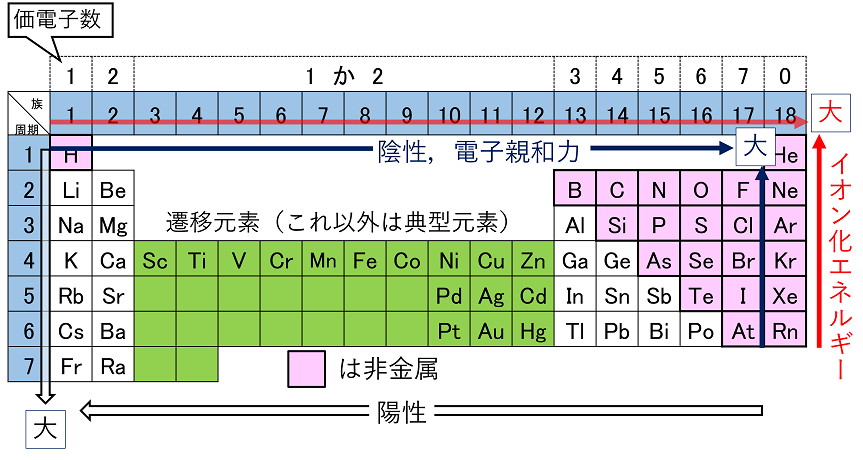
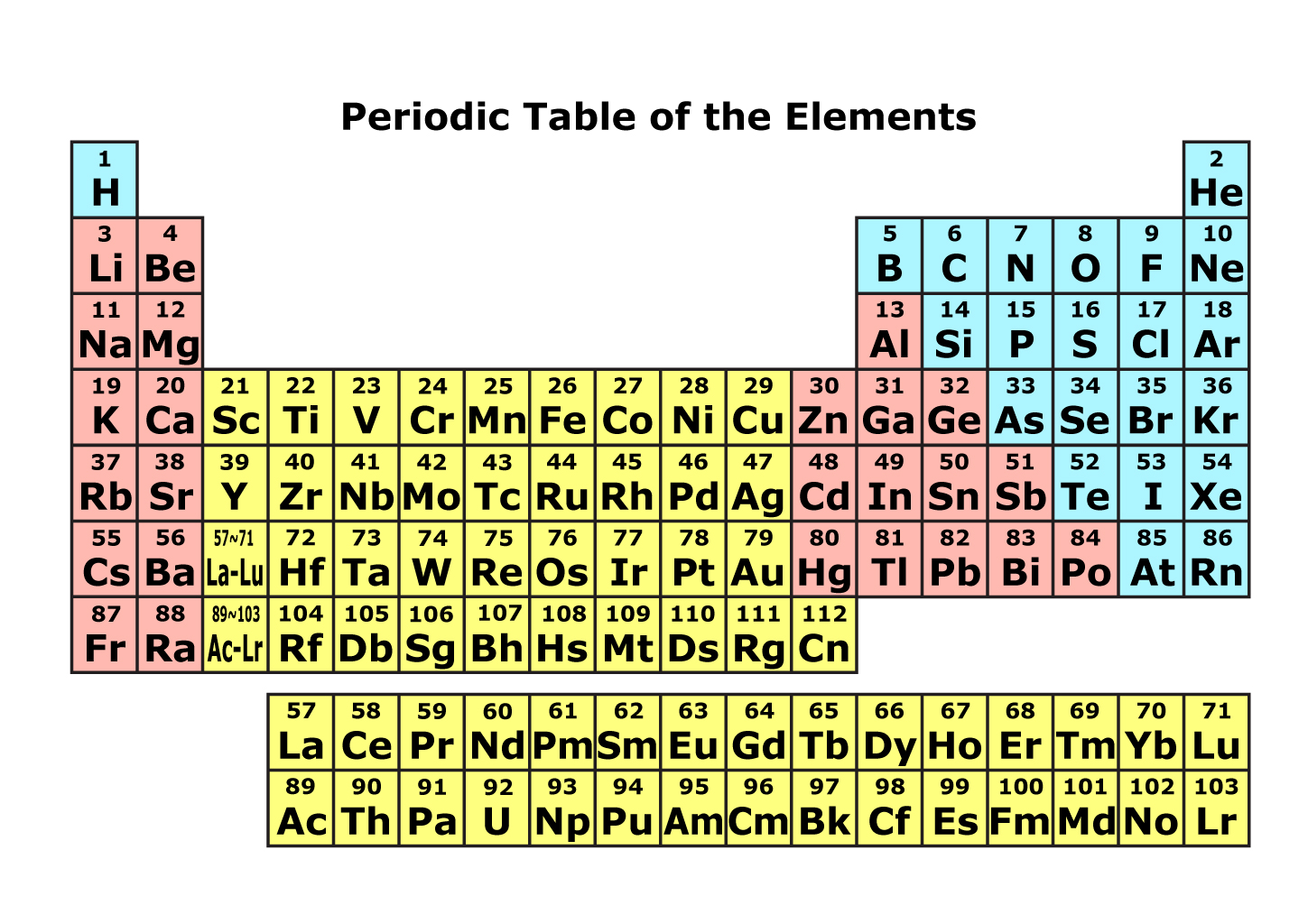


 電気陽性
電気陽性










