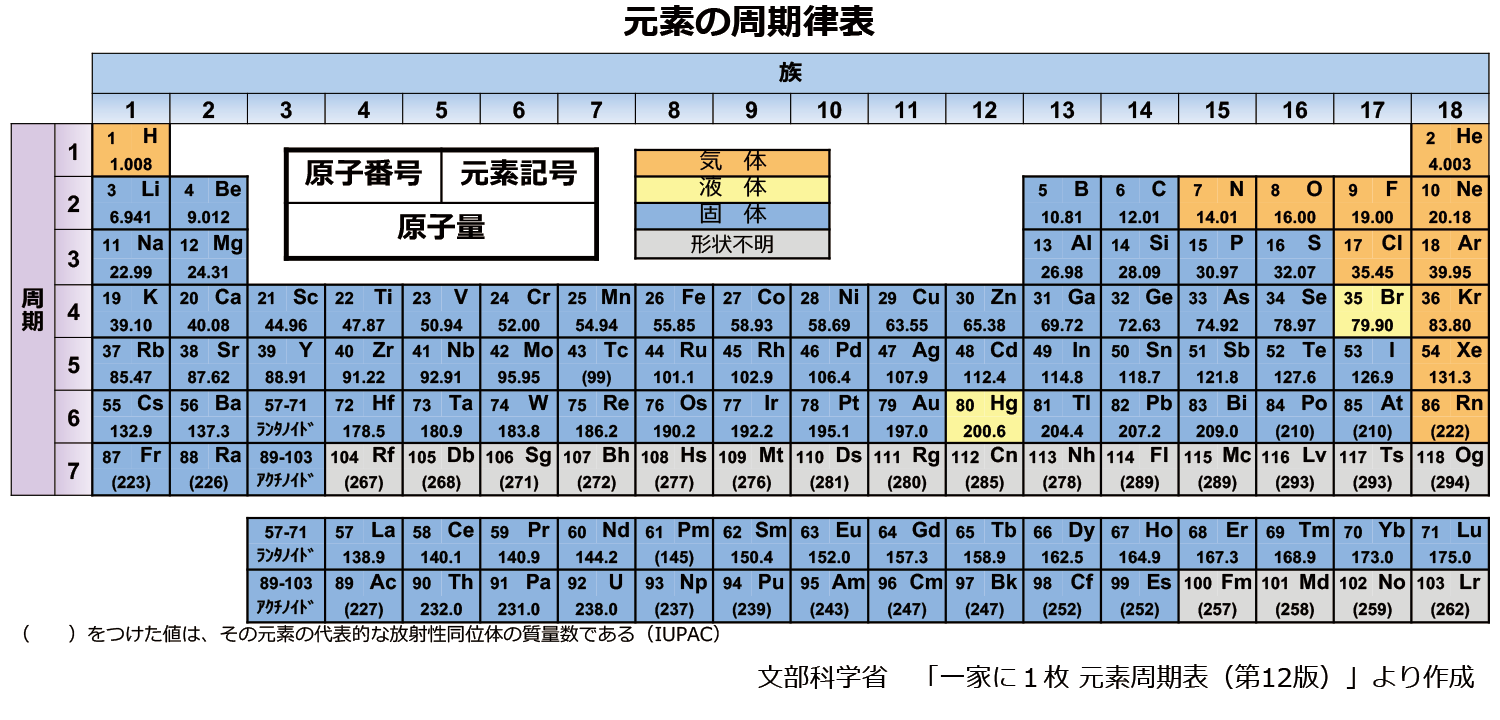
化学元素の周期表は 、どの金属が金属であるか、どれが最も密度が高く、最も重く、最も反応性が高いかを確認するなど、元素の特性を知りたい場合に優れた情報源として知られています。しかし、 周期表は 常に組織化され、完全であるとは限りませんでした。元素をその類似性に基づいて配置することは、すでに多くの議論と科学的研究の対象となっており、現在の周期表はより効率的ではありますが、その形成は他の多くのより原始的なものに由来しています。もの。
この記事の内容

ドーベライナーの分類 – トライアドの法則 (1829)
ドイツの科学者ヨハン W. ドーベライナー (1780-1849) は、多くの元素が原子質量との類似性に従って 3 つずつ 3 つ (トライアッド) に分類できることを観察しました。
-
近接性
Fe = 56u
Co = 59u
Ni = 58u
ご覧のとおり、鉄、 コバルト 、 ニッケルは 非常によく似た原子量を持っています。 -
公差
リー = 7u
Na = 23u
K = 39u
連続する要素の質量の差は昇順で 16 に等しいことに注意してください。実際には、23 – 7 = 16、つまり 23 – 7 = 16 となります。 39 – 23 = 16。 -
算術平均
Ca = 40u
Sr = 88u
Ba = 137u
カルシウム と バリウム の質量の算術平均を取ると、 ストロンチウム のおおよその原子質量が得られます: 137+40 = 177。 177/2 = 88.5。

シャンクルトワの分類 – テルリックねじ (1862)
フランスの 地質学者 、アレクサンダー ベギュイエ ド シャンクルトワ (1820-1886) は、要素を次のように整理しました。最初に、彼は円柱の表面を 16 個の柱と無数の水平柱に分割しました。質量 16u を酸素に割り当てました。酸素 (点 0) から始まり 16 番目に重い元素で終わるらせん状の線を、線が到達する限り描きました。この手順を、すべての要素が分割線に割り当てられるまで繰り返しました。
テーブルは次のようになります。

ニューランズの分類 – オクターブの法則 (1864)
英国の化学教授で実業家であるジョン AR ニューランズ (1838-1898) は、元素を原子量の増加順に 7 つのグループに並べて分類することを考案しました。彼はすぐに、その化学的性質が、オクターブごとに繰り返される音符のように、左から右に数えて 1 番目と 8 番目の元素に似ていることに気づきました。

古い分類と現在のモデルの失敗
有望であるにもかかわらず、要素を分類するための古いモデルには多くの非互換性がありました。
-
トライアドの法則
この配布方法は制限が多すぎて特定の要素のみを提供するため、効果がないと考えられていました。 -
テルリックスクリュー
原子質量の値はしばしば誤りがあり、不正確であるため、この方法の受け入れは低かった。 -
オクターブの法則
このモデルもまた、原子質量の値に問題があるとして禁止されました。言い換えれば、一部の元素は間違った場所にありました。たとえば、 塩素 や フッ素 はコバルトやニッケルに似た特性を持っていません。
成功しなかったにもかかわらず、これらのモデルは化学元素の分類の継続的な改善に貢献しました。
ジュリアス・ローター・マイヤー (1830-1895) と ドミトリ・イワノビッチ・メンデレーエフ (1834-1907) という 2 人の科学者が互いに孤立して研究しましたが、同様の結果に達しました。メンデレーエフの研究はより大胆でした。
メンデレーエフは、元素を分類するためのモデルを王立ロシア化学会に提出し、広く受け入れられました。あなたの理論は、いくつかの観察によって確認できます。
- 「これらの元素を原子質量に従って配置すると、明らかな周期的特性が明らかになります。
- まだまだ未知の要素が数多く発見されることを期待しなければなりません。たとえば、 アルミニウム (eka-Aluminum) やシリコン (exa-Silicon) に類似した元素で、その原子質量は 65 ~ 75 インチになります。
言い換えれば、 メンデレーエフは、 元素の特性 は原子質量の周期関数であると述べました。

1869 年にメンデレーエフによって作成された周期表。新しい元素を含めるための空きスペースが示されています。
現在の周期表はメンデレーエフの周期表の忠実なコピーではなく、より改良されたものです。それは、元素が意図された空きスペースを占める元素の出現によるものではなく、1913 年に確立された概念、つまり原子番号によるものです。
ヘンリー GL モーズリーは、元素の正体はその質量に直接関係するのではなく、それを表す原子の核電荷に関係すると定義しました。 したがって、彼はメンデレーエフが提案した表をわずかに修正し、今日までその本質を残しています。
サルデッラ、アントニオ。化学コース: 一般化学、サンパウロ – SP: Editora Ática、2002。第 25 版、第 2 刷。 448ページ。
http://pt.wikipedia.org/wiki/História_da_Table_Periódica (2010 年 3 月 19 日にアクセス)
http://www.10emtudo.com.br/imprimir_artigo.asp?CodigoArtigo=10 (2010 年 3 月 19 日にアクセス)
http://web.fccj.org/~ethall/period/period.htm (2010 年 3 月 19 日にアクセス)
ギャラリー